Introducción al Cáncer Gástrico y la Necesidad de Paliación
El cáncer gástrico representa una de las principales causas de mortalidad por cáncer a nivel mundial y la primera causa de muerte por neoplasia maligna en Colombia. A pesar de los avances en la comprensión de sus causas, la prevención efectiva sigue siendo un desafío. Tradicionalmente, la cirugía ha sido la principal alternativa para intentar curar la enfermedad, pero en los últimos años, la endoscopia y la laparoscopia han emergido como opciones válidas para el manejo curativo. En cuanto a las terapias adyuvantes, la radioterapia combinada con quimioterapia postoperatoria y la quimioterapia perioperatoria han demostrado mejorar significativamente la supervivencia. El tratamiento del cáncer gástrico es, por lo tanto, individualizado, multimodal y multidisciplinario, requiriendo la evaluación por un equipo oncológico altamente especializado.
Aunque la incidencia global del cáncer gástrico está disminuyendo, varía geográficamente de manera significativa. Países como Bulgaria, Colombia, China, Japón y Portugal presentan las tasas más altas de mortalidad ajustada, mientras que en Estados Unidos, India y la mayoría de los países africanos, esta neoplasia es menos relevante. La tasa de mortalidad en Chile, por ejemplo, es del 20 por 100.000 habitantes, siendo la principal causa de muerte por tumores malignos, con variaciones regionales dentro del país.
La etiopatogenia del cáncer gástrico es multifactorial, involucrando factores dietéticos (nitratos, grasas animales, sal, baja ingesta de antioxidantes), la infección crónica por Helicobacter pylori, el tabaquismo y factores socioeconómicos. Se distinguen dos formas microscópicas: la intestinal, asociada a factores ambientales y dietéticos, y la difusa, más indiferenciada, de debut temprano y con peor pronóstico. Se postula un desarrollo escalonado para la variedad intestinal, desde mucosa normal hasta carcinoma, con la inflamación crónica por H. pylori como desencadenante inicial. La variedad difusa no sigue un patrón histopatológico similar conocido.
Además de los factores ambientales y dietéticos, existen condiciones mórbidas predisponentes como el esófago de Barrett, gastritis atrófica, anemia perniciosa y metaplasia intestinal. Los adenomas gástricos mayores de 2 cm tienen indicación de resección, y el cáncer gástrico del muñón, que aparece años después de una gastrectomía subtotal, requiere control endoscópico. Los factores hereditarios, como la mutación del gen de la E-Cadherina, también juegan un papel, manifestándose en individuos jóvenes con la variedad difusa.
El cáncer gástrico incipiente, que compromete la mucosa o submucosa, es asintomático en el 80% de los casos. Cuando hay síntomas, suelen ser inespecíficos, similares a un síndrome ulceroso. En estadios avanzados, la sintomatología es más florida, incluyendo dolor abdominal, pérdida de peso, anorexia, náuseas, vómitos y disfagia. El diagnóstico se realiza principalmente mediante endoscopia digestiva alta con biopsia, complementada en ocasiones por radiología con doble contraste. La estadificación incluye tomografía axial computada de abdomen y pelvis, y en casos de sospecha de carcinomatosis, laparoscopia de estadificación.
El Concepto de Paliación y el Papel de la Endoscopia
El verbo "paliar" se define como mitigar, suavizar o atenuar la violencia de una enfermedad. Los cuidados paliativos, según la Organización Mundial de la Salud, son aquellos cuidados apropiados para pacientes con enfermedades avanzadas y progresivas, donde el control del dolor y otros síntomas, junto con los aspectos psicosociales y espirituales, cobran suma importancia. El objetivo es lograr la mejor calidad de vida posible para el paciente y su familia. La medicina paliativa considera la vida y la muerte como procesos normales, ofreciendo un sistema de apoyo integral.
En el contexto del cáncer gástrico sin opción curativa, los tratamientos paliativos endoscópicos pueden ser cruciales para aliviar la obstrucción que genera síntomas como sed y vómitos. Si bien la cirugía tradicional, la quimioterapia y la radioterapia son herramientas válidas, las prótesis autoexpandibles (PAE) se han convertido en un pilar fundamental del tratamiento paliativo. Otras técnicas como el láser, la coagulación con argón plasma, la terapia fotodinámica, la braquiterapia y la inyección de sustancias han sido descritas, pero su popularidad ha sido limitada por discutible efectividad, necesidad de múltiples procedimientos, dificultades logísticas y alto costo.
Prótesis Autoexpandibles (PAE): Avances Tecnológicos y Tipos
El desarrollo tecnológico ha impulsado la evolución de las prótesis autoexpandibles (stent). Estos dispositivos tubulares en forma de malla se pliegan para facilitar su inserción a través de estenosis importantes, sin necesidad de dilatarlas previamente en la mayoría de los casos. Una vez liberada en la zona obstruida, la PAE se expande, logrando un diámetro suficiente para recanalizar la zona estrecha.
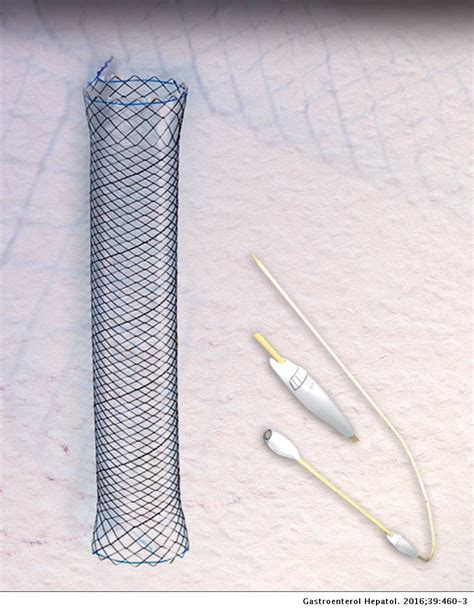
Existen diversos tipos de prótesis:
- Prótesis plásticas de silicona.
- Prótesis elaboradas con materiales bioabsorbibles.
- Prótesis metálicas de nitinol: Son las más utilizadas en patología oncológica avanzada debido a sus pequeños diámetros de introducción y a que su integración íntima con el tejido no es un problema en pacientes con corta sobrevida.
Dentro de las prótesis metálicas, existen numerosos diseños con características específicas:
- Tejido para favorecer el anclaje y disminuir la tasa de migración.
- Sistemas de recubrimiento plástico para prevenir el crecimiento tumoral dentro de la prótesis.
- Prótesis con válvula antirreflujo, diseñadas para prevenir el reflujo gastroesofágico en casos donde la prótesis sobrepasa el esfínter esofágico inferior.
Las prótesis recubiertas previenen sustancialmente el crecimiento intraluminal del tumor, pero pueden asociarse a un aumento significativo en la tasa de migración. La efectividad de las prótesis con válvula antirreflujo para prevenir el reflujo secundario a la omisión del esfínter esofágico inferior no ha sido contundentemente demostrada. Estudios recientes sugieren que las prótesis autoexpandibles de silicona, aunque proporcionan una paliación comparable a las metálicas, se asocian a una mayor tasa de migración.
Consideraciones y Aspectos Técnicos en la Indicación de PAE
La evidencia científica que soporta la indicación de tratamiento paliativo en cáncer gástrico es escasa, lo que a menudo lleva a decisiones basadas en percepciones subjetivas y experiencias combinadas. Tradicionalmente, el riesgo perioperatorio de la cirugía paliativa solo se justifica si se espera una sobrevida mayor a 30 días. Las PAE desafían esta noción, ya que su mínimo riesgo perioperatorio las hace aceptables incluso en pacientes con esperanza de vida corta, siempre que no comprometan la vida o la calidad de vida posprocedimiento.
La instalación endoscópica de PAE se sustenta en evidencia más o menos clara dentro del complejo panorama de la indicación de procedimientos paliativos. Cuando está bien indicada y realizada, la colocación de una PAE es una terapia costo-efectiva y segura para la paliación de la obstrucción maligna del tracto digestivo superior. La decisión de indicar o contraindicar una PAE debe ser resultado del acuerdo entre el equipo tratante y el paciente/familia, con claridad sobre las expectativas reales de la enfermedad y el balance riesgo-beneficio.
Desde el punto de vista técnico, el beneficio buscado con la PAE es la tolerancia de alimentos líquidos o papillas, y en tumores distales, la mejoría del vómito. La indicación se da en un intervalo de tiempo específico y corto de la enfermedad, cuando la estrechez tumoral es lo suficientemente importante para causar disfagia pero permite el paso seguro de los instrumentos endoscópicos sin necesidad de dilataciones mecánicas. El paso más determinante es lograr atravesar la estenosis tumoral con una guía y situarla más allá de la obstrucción, sobre la cual se dirige la prótesis plegada.
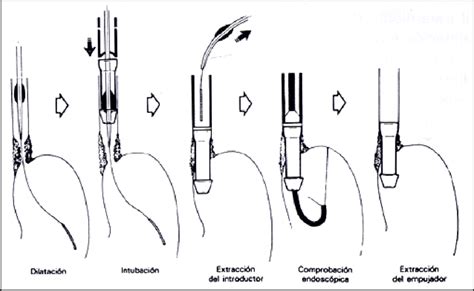
Si el endoscopio de pequeño calibre pasa a través de la estenosis, puede asegurar la posición de la guía distal. Sin embargo, es deseable contar con confirmación y guía fluoroscópica en todos los procedimientos. En tumores del esófago distal, la colocación es más simple debido a su estructura rectilínea. En el confluente píloro-duodenal, más tortuoso y móvil, se recomienda marcar radiológicamente el inicio y fin de la estenosis, y usar inyecciones submucosas de medio de contraste.
Para tumores distales, se recomiendan PAE con mecanismos de liberación delgados para inserción a través del canal de trabajo del endoscopio, lo que facilita el reposicionamiento en regiones anatómicas móviles. El estudio de vías digestivas altas puede aportar información valiosa sobre la extensión y características de la estenosis si el abordaje endoscópico transestenótico no es posible. Aunque la dilatación transtumoral es ocasionalmente necesaria, lo ideal es que la PAE realice la dilatación gradual de la estenosis.
Complicaciones y Evidencia Científica
Las complicaciones graves de la colocación de PAE son raras, pero suelen indicar una intervención urgente y de alto riesgo. Incluyen perforaciones, migración distal y fístulas secundarias. La migración distal es una complicación tardía que puede requerir la retirada del cuerpo extraño para evitar obstrucción o perforación. La obstrucción por crecimiento tumoral puede solucionarse insertando nuevas prótesis recubiertas, aunque estas tienden a migrar más distalmente.
La evidencia científica sobre el tratamiento paliativo en cáncer gástrico distal obstructivo, comparando PAE con gastroyeyunostomía, sugiere que las PAE tienen una mayor probabilidad de éxito clínico, un menor tiempo de restablecimiento de la vía oral, una menor probabilidad global de complicaciones y un menor tiempo de hospitalización. En el cáncer de la unión esófago-gástrica, la inserción de PAE es segura, efectiva y más rápida para aliviar la disfagia en comparación con otros tratamientos endoscópicos. Para pacientes con buen estado funcional que no requieren alivio inmediato, la braquiterapia intraluminal de dosis alta es una alternativa apropiada que puede alargar la supervivencia libre de síntomas. La inserción de PAE y la braquiterapia son preferibles a otros tratamientos ablativos endoscópicos debido a la menor necesidad de reintervenciones.
Colocación de Gastrostomía Endoscópica Percutánea (GEP)
Resumen de la Evidencia y Conclusiones
El cáncer gástrico es la primera causa de muerte por tumores malignos en Chile y la segunda a nivel mundial. A pesar de los avances en la comprensión de sus causas, la prevención efectiva sigue siendo un objetivo distante. Las mayores novedades se encuentran en el tratamiento, donde la cirugía radical sigue siendo el pilar fundamental, pero la endoscopia y la laparoscopia han emergido como alternativas válidas. Las terapias adyuvantes, como la quimioterapia y la radioterapia, juegan un papel importante en mejorar la supervivencia. El tratamiento del cáncer gástrico es un enfoque individualizado, multimodal y multidisciplinario.
En la paliación del cáncer gástrico avanzado, especialmente en casos de obstrucción, las prótesis autoexpandibles (PAE) ofrecen una alternativa segura y efectiva. La evidencia sugiere que las PAE son superiores a la gastroyeyunostomía en términos de éxito clínico, tiempo de recuperación y complicaciones, y son una opción preferible para el alivio de la disfagia en comparación con otros tratamientos endoscópicos. La decisión de utilizar una PAE debe basarse en una cuidadosa evaluación del paciente, la enfermedad y el balance riesgo-beneficio, en un esfuerzo colaborativo entre el equipo médico y el paciente/familia.
tags: #tratamiento #paliativo #cancer #gastrico