La comprensión de la vulnerabilidad neuronal específica es crucial para el desarrollo de terapias efectivas contra enfermedades neurodegenerativas como el Parkinson y el Alzheimer. Estas enfermedades se caracterizan por la afectación selectiva de ciertos grupos neuronales, lo que conduce a la manifestación de síntomas motores y no motores.
Enfermedad de Parkinson: Vulnerabilidad de Neuronas Dopaminérgicas
Características Generales de la Enfermedad de Parkinson (EP)
La enfermedad de Parkinson (EP) es el segundo proceso neurodegenerativo más frecuente en la población mayor de 65 años. Se prevé que su incidencia aumentará considerablemente con el progresivo envejecimiento poblacional en los próximos años, estimándose un incremento de la prevalencia mundial de 6,9 millones de personas en 2015 a 14 millones en 2040.
El diagnóstico de la EP se realiza, en la mayoría de los casos, cuando la pérdida de neuronas de la sustancia negra pars compacta (SNc) alcanza un 50-60% y la pérdida de dopamina en el estriado es de un 70-80%. Esto coincide con la aparición de los signos motores clásicos de la enfermedad: temblor, rigidez y lentitud de movimientos (bradicinesia). Estas manifestaciones suelen tener un inicio unilateral y asimétrico, y muestran una mejoría marcada con el tratamiento dopaminérgico.
Además de los signos motores, una proporción significativa de pacientes presenta síntomas no motores, generalmente asociados a la alteración de regiones no dopaminérgicas. Estos síntomas pueden surgir con marcada antelación (ej. 10-15 años antes del diagnóstico), alrededor del diagnóstico o posteriormente. Los síntomas no motores incluyen alteraciones gastrointestinales (como estreñimiento o retraso en el vaciamiento gástrico), disautonomía (como nicturia o disfunción sexual), alteraciones sensitivas (como anosmia o dolor), trastornos del sueño (trastornos del comportamiento del sueño REM o insomnio) y signos neuropsiquiátricos (como depresión, apatía o déficits cognitivos).
El periodo premotor, caracterizado por síntomas como estreñimiento, hiposmia, trastornos del sueño REM y depresión, representa una ventana temporal fundamental para el estudio del proceso fisiopatológico subyacente y para la aplicación de tratamientos modificadores que permitan la prevención o el retraso del desarrollo y la progresión de la EP.
Características Histopatológicas de la EP
Desde el punto de vista histopatológico, la EP se caracteriza por la degeneración de las neuronas dopaminérgicas situadas en la SNc, lo que se asocia estrechamente a la aparición de los signos motores parkinsonianos. La degeneración dopaminérgica afecta principalmente a la región caudoventrolateral de la SNc (grupo dopaminérgico A9) y progresa hacia regiones más rostrodorsomediales. Los signos motores no aparecen hasta que la depleción de neuronas dopaminérgicas de la SNc es del 50-60% y la denervación dopaminérgica estriatal es del 70-80%.
Otros grupos dopaminérgicos, como el área retrorrubral (A8) o el área tegmental ventral (VTA, A10), presentan una afectación más leve. El proceso neurodegenerativo en la EP también afecta a núcleos no dopaminérgicos como el locus coeruleus (LC), el núcleo basal de Meynert (NBM), el núcleo pedunculopontino (PPT), el núcleo motor dorsal del vago (NMDV), los núcleos del rafe, la amígdala y el hipocampo, afectando así a otros sistemas como el noradrenérgico y el serotoninérgico.
La otra característica histopatológica es la presencia de inclusiones intraneuronales llamadas cuerpos de Lewy, compuestos principalmente por el plegamiento aberrante de la proteína alfa-sinucleína, junto con otras proteínas como la ubiquitina y la proteína p62. El depósito citoplasmático de los cuerpos de Lewy no se limita solo a la SNc, sino a otras regiones del sistema nervioso central y periférico, proponiéndose un patrón de progresión topográfico con inicio en el bulbo raquídeo y progresión caudocraneal.
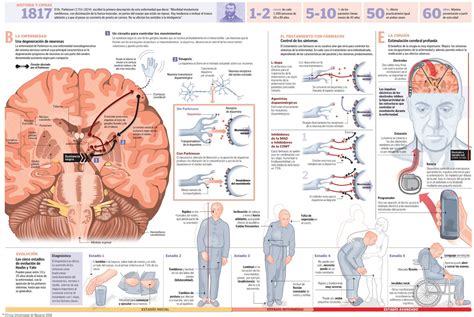
Pérdida Neuronal y Territorios Anatómicos Vulnerables
En la EP, existe una pérdida inicial y predominante de neuronas dopaminérgicas de la SNc que proyectan al estriado, causando una depleción de dopamina (DA) en esta región. En pacientes tempranos con EP, la tomografía por emisión de positrones (PET) revela que la región que primero pierde DA es la parte más dorsal del putamen postcomisural. Es fundamental atender a la SNc y el putamen dorsal para desarrollar terapias neuroprotectoras en estadios iniciales de la EP.
Además de la SNc, la acumulación de cuerpos de Lewy y la muerte neuronal afectan a otros núcleos del sistema nervioso central y periférico. Se ven afectadas las neuronas colinérgicas del núcleo PPT, del NBM y del núcleo DMV, las neuronas noradrenérgicas del LC y las neuronas serotoninérgicas del núcleo del rafe. Algunos estudios muestran alteraciones en el número de neuronas en núcleos talámicos como el núcleo centromediano-parafascicular, el hipotálamo, el hipocampo y el bulbo olfatorio. La afectación de estos núcleos se correlaciona con la progresión de los síntomas no motores.
Los núcleos que presentan agregados de cuerpos de Lewy en la EP incluyen la corteza cerebral, el hipotálamo, el núcleo basal de Meynert, la SNc, los núcleos del rafe, el LC, el DMV y los ganglios simpáticos.
Heterogeneidad y Vulnerabilidad Selectiva de Neuronas Dopaminérgicas
Dentro de los grupos neuronales dopaminérgicos, existe una gran heterogeneidad en términos de morfología, metabolismo, patrones moleculares, acumulación de proteínas, niveles de inflamación y expresión de proteínas. En esta revisión se exponen los hallazgos de distintos factores que podrían explicar la especial vulnerabilidad de determinadas neuronas dopaminérgicas de la SNc.
Conocer los mecanismos y factores subyacentes a la vulnerabilidad selectiva de las neuronas dopaminérgicas de la región ventrolateral de la SNc es imprescindible para desarrollar terapias neuromoduladoras y/o neuroprotectoras efectivas que frenen o modifiquen el proceso neurodegenerativo en la EP.
Vía Nigroestriatal y Otras Proyecciones Dopaminérgicas
El circuito nigroestriatal está topográficamente organizado. Las neuronas de las regiones ventrolaterales y posteriores de la SNc proyectan principalmente al putamen posterior (motor), mientras que las células más mediales de la SNc proyectan al putamen anterior y a la cabeza del caudado. Estas proyecciones forman generalmente grupos independientes que se sobreponen, indicando una falta de organización topográfica precisa.
El estriado y la SNc forman un circuito estriato-nigro-estriatal con tres circuitos paralelos relacionados con las regiones límbica, asociativa y motora del estriado. Estudios recientes indican que las proyecciones nigro-extraestriatales también muestran una organización similar. Además, se ha demostrado un circuito nigro-estriato-nigral en el que los estriosomas proyectan a la región ventral de la SNc y estas proyectan de vuelta a las regiones dorsales del estriado.
El mayor número de neuronas dopaminérgicas se encuentra en la SNc y en el VTA.
Fisiologia de la dopamina y las vias dopaminergicas
Vulnerabilidad Neuronal Específica en la Enfermedad de Alzheimer
La neurodegeneración provocada por la enfermedad de Alzheimer es un proceso paulatino que varía de acuerdo a su gravedad. Los investigadores han identificado un grupo de “neuronas vulnerables” que son las primeras en sufrir la degradación que produce esta enfermedad.
Un estudio reciente avanza sobre el funcionamiento interno de este subconjunto de neuronas y describe los factores moleculares que hacen que las células cerebrales entorrinales sean especialmente sensibles a la degeneración. El resultado es una breve lista de genes que podrían representar nuevos objetivos de tratamiento farmacológicos.
El primer signo de Alzheimer es la acumulación de péptidos Aβ, que forman placas en todo el cerebro. El segundo signo de la enfermedad es una mezcla de proteínas tau conocidas como ovillos neurofibrilares que se forman después de la acumulación de placas y obstruyen el interior de las neuronas. A diferencia de las placas amiloides, este último grupo de proteínas inicialmente se agrupa únicamente dentro de un grupo distinto de células de la corteza entorrinal.
La mayor barrera para estudiar estas células cerebrales fue la ausencia de una forma fácil de distinguir las neuronas vulnerables de sus vecinas. Con la técnica BacTRAP, los investigadores pudieron aislar las neuronas vulnerables y analizar cómo difieren genéticamente de las células cerebrales más resistentes.
Se cree que el gen que produce una proteína llamada PTBP1, un factor de empalme que dirige a las células a crear uno de los dos subtipos de proteína tau, desempeña un papel importante en las primeras etapas de la enfermedad de Alzheimer, determinando si las proteínas tau se agrupan en ovillos neurofibrilares en primer lugar. Al descubrir qué hace que las neuronas sean más vulnerables, se pueden abrir múltiples vías para disminuir su vulnerabilidad.
Circuitos Neuronales y Procesamiento de Información Social
Para examinar los mecanismos neuronales que sustentan la selección y separación de la información social relevante para la tarea, un equipo de investigadores llevó a cabo un experimento con 30 participantes. Cada uno completó una tarea de comparación social, durante la cual se registró su actividad cerebral mediante resonancia magnética funcional (RMf).
Cuando analizaron los escáneres recogidos, descubrieron que dos regiones cerebrales estaban particularmente activas mientras los participantes completaban la tarea de comparación social. Así descubrieron que cuando a la gente le resulta difícil comparar a otros en la dimensión relevante (los dos personajes a comparar son similares) utiliza la información irrelevante para hacerlo.
A nivel neuronal, descubrieron un área cerebral en el córtex prefrontal medial que minimiza el impacto de la información irrelevante en nuestra toma de decisiones. El reciente trabajo de este equipo de investigadores señala un circuito neuronal que podría subyacer a la valiosa capacidad de los seres humanos para ordenar selectivamente la información social y centrarse en habilidades o cualidades específicas de los demás en función del contexto en el que se encuentren.
tags: #grupo #neuronales #vulnerables #especificos