La vejiga hiperactiva (VH) es una condición que afecta a un número significativo de personas, y su comprensión ha avanzado considerablemente en los últimos años. Estudios han revelado un vínculo entre el síndrome metabólico y la VH, especialmente en casos de obesidad.
Relación entre Síndrome Metabólico y Vejiga Hiperactiva
Se ha demostrado que la mayoría de las opciones de tratamiento convencionales para la VH, como los antimuscarínicos, la neuromodulación sacra (SNM) y la toxina botulínica, son menos efectivas en pacientes con síndrome metabólico o en comparación con otras poblaciones de pacientes. Por el contrario, el mirabegrón, un agonista de los receptores β3-adrenérgicos, diseñado inicialmente como medicamento contra la obesidad, ha mostrado ser igualmente efectivo en pacientes obesos y no obesos con VH, resultando muy adecuado para esta población. No obstante, puede ser necesario un ajuste de la dosis en ciertos casos.
Además, el tadalafilo, un inhibidor de la fosfodiesterasa, ha demostrado ser un tratamiento eficaz y bien tolerado para la VH en mujeres. Dada la implicación de las vías del estrés inflamatorio y oxidativo en pacientes con síndrome metabólico y VH, los inhibidores de la fosfodiesterasa podrían convertirse en una opción terapéutica relevante para estos pacientes, como sugieren estudios en modelos animales y ensayos clínicos preliminares.
Factores Psicológicos y Trastornos Afectivos
Existe una interconexión entre la VH y la salud mental. El impacto de la VH puede predisponer a los individuos a la ansiedad y la depresión. Datos recientes sugieren una relación bidireccional, donde el estrés emocional y un historial de ansiedad o depresión pueden ser factores de riesgo para el desarrollo de la VH en mujeres. Mecanismos biológicos comunes podrían subyacer a la coexistencia de ambos trastornos.
Se ha investigado el factor liberador de corticotropina (CRF) como un posible contribuyente fisiopatológico común a la VH y la ansiedad o depresión. Asimismo, la depleción de serotonina se postula como otro candidato común, dado su papel establecido en los trastornos afectivos y los hallazgos experimentales que vinculan la reducción de serotonina con un incremento de la frecuencia urinaria y la hiperactividad del detrusor.
Las disfunciones de los canales receptores de potencial transitorio (TRP) y la sensibilización central también se consideran cofactores fisiopatológicos comunes de la ansiedad, la depresión y la VH. La sensibilización central se define como un aumento de la actividad sináptica en las neuronas somatosensoriales de la médula espinal, resultando en una respuesta amplificada ante estímulos.
Muchos de estos mecanismos fisiopatológicos pueden ser compartidos por la VH inducida por estrés social y los fenotipos de VH asociados a trastornos funcionales gastrointestinales o comunicación cruzada entre órganos pélvicos. Tratamientos como la duloxetina, los antagonistas de los TRP vaniloides (TRPV) o los antagonistas de CRF podrían dirigirse a estas bases biológicas compartidas.
Rol de las Hormonas Sexuales
La deficiencia de hormonas sexuales en mujeres tiene un impacto claro en el tracto urinario inferior, relacionado con la presencia de receptores de estrógenos y progesterona en la uretra, vejiga y músculos del suelo pélvico. Estudios epidemiológicos respaldan el papel de la deficiencia hormonal en la etiopatogénesis de los síntomas del tracto urinario inferior (STUI), con un alto porcentaje de mujeres relacionando el inicio de la incontinencia urinaria con la menopausia.
La deprivación de estrógenos puede influir en la urgencia urinaria a través de diversos mecanismos, como el aumento de la contractilidad del detrusor, la liberación de acetilcolina, cambios en la señalización urotelial o el aumento de la expresión de la conexina 43. La VH en estas pacientes se asocia frecuentemente con infecciones urinarias y síntomas vulvovaginales, definidos como el síndrome genitourinario de la menopausia.
El uso de estrógenos vaginales puede mejorar la incontinencia urinaria, especialmente la incontinencia urinaria de urgencia (IUU), aunque su relevancia puede ser cuestionable en mujeres sin atrofia vaginal. En comparación con las mujeres, los datos sobre la deficiencia de hormonas sexuales como causa de VH en varones son escasos, pero estudios sugieren que la testosterona podría disminuir la excitabilidad del detrusor y tener un impacto en la liberación de mediadores uroteliales.
Microbiota Urinaria y su Impacto
Investigaciones recientes sugieren la existencia de comunidades microbianas en el tracto urinario humano, denominadas microbiota urinaria, desafiando la creencia tradicional de que la orina es estéril. La microbiota urinaria podría desempeñar un papel en la patogénesis de la VH, aunque los mecanismos y las implicaciones terapéuticas aún no están claros.
Se ha detectado ADN bacteriano y una mayor concentración bacteriana en pacientes con IUU, junto con una posible disminución de la diversidad del microbioma urinario. Ciertas especies de Lactobacillus, como Lactobacillus crispatus, podrían ser marcadores de una vejiga femenina sana, y su menor carga en pacientes con IUU sugiere un papel protector en el tracto urinario inferior al mantener un ambiente ácido que inhibe el crecimiento de bacterias virulentas.
Aunque la administración intravaginal de Lactobacillus es prometedora para la prevención de infecciones recurrentes del tracto urinario inferior (ITU), no se han investigado sus efectos en la VH. Estudios preliminares sugieren un impacto significativo del microbioma urinario en la respuesta a diversos tratamientos de VH, como antimuscarínicos o toxina botulínica. Algunos estudios indican que los respondedores a estos tratamientos podrían tener menos bacterias y una menor diversidad microbiana.
Un microbioma urinario aberrante, con menor diversidad, se ha correlacionado positivamente con niveles más altos de depresión y ansiedad, sugiriendo una comunicación entre la microbiota urinaria y el cerebro, similar a la del eje intestino-cerebro. Esto plantea la hipótesis de un eje cerebro-vejiga-microbiota, que podría implicar mecanismos de comunicación bidireccional y estar integrado en un eje más global cerebro-intestino-vejiga-microbiota a través de la sensibilización central.
Comunicación entre Órganos Pélvicos: El Eje Intestino-Vejiga
La vejiga y el colon-recto comparten un origen embriológico común, desarrollando vías neurales espinales con aferentes que inervan ambos órganos y convergen en la misma raíz de ganglio dorsal. Esto permite mecanismos de comunicación entre la vejiga y el colon, y puede ser el impulso de la sensibilización cruzada, donde la sensibilización de los nervios de un órgano pélvico se ve afectada por una lesión aguda en otro.
Se han sugerido relaciones bidireccionales entre la VH y la incontinencia fecal o el estreñimiento. El síndrome del intestino irritable (SII) es la afección gastrointestinal más frecuentemente relacionada con la VH, con una alta prevalencia de SII en pacientes con VH.
El interés en el papel de la sensibilización central en la coexistencia de trastornos urológicos y gastrointestinales funcionales ha aumentado. Esta sensibilización central puede ser activada por la sensibilización cruzada de los órganos pélvicos, conduciendo a una amplificación de la señalización en la médula espinal y el cerebro. Algunos autores sugieren que la sensibilización central podría ser una disfunción primaria que da lugar a la coexistencia de trastornos funcionales gastrointestinales y urológicos, junto con trastornos afectivos, como parte de un eje cerebro-intestino-vejiga.
Este fenotipo de VH del eje cerebro-intestino-vejiga puede ser inducido por el estrés. Tratamientos dirigidos tanto a la vejiga como al intestino, como la SNM o la estimulación percutánea del nervio tibial posterior (PTNS), podrían ser beneficiosos. La duloxetina también podría ser una opción terapéutica futura para el abordaje de pacientes con "eje cerebro-intestino-vejiga-VH", al dirigirse a la sensibilización central.
El Sistema Nervioso Autónomo y la Vejiga Hiperactiva
El sistema nervioso autónomo (SNA) regula procesos corporales involuntarios como la presión arterial y la frecuencia respiratoria. Sus divisiones principales son el sistema simpático y el sistema parasimpático.
Se ha postulado que la disfunción subclínica del sistema nervioso autónomo podría ser un factor causante de la VH "idiopática". Estudios han confirmado un desequilibrio autónomo asociado a la VH, con predominio de la actividad parasimpática cuando la vejiga está vacía y de la actividad simpática al final del llenado en mujeres con VH. Esto podría indicar que el llenado vesical induce una respuesta simpática global.
Algunos estudios sugieren que la disfunción simpática podría predominar sobre la disfunción parasimpática en pacientes con VH, y que estos pacientes podrían ser menos propensos a presentar hiperactividad del detrusor en estudios urodinámicos. Si bien otros estudios han comunicado alteraciones similares de la actividad simpática, también se ha observado una relación entre la VH y una mayor activación parasimpática. Curiosamente, los antimuscarínicos podrían reducir la disfunción parasimpática y mejorar los síntomas de la VH.
Por otro lado, la disfunción simpática en pacientes con VH podría predecir una escasa respuesta a los antimuscarínicos, sugiriendo un posible papel de los agonistas β3 en la restitución de la activación de las vías simpáticas eferentes cuya disfunción genera la inhibición del músculo detrusor.
Enfoques Diagnósticos y Terapéuticos Futuros
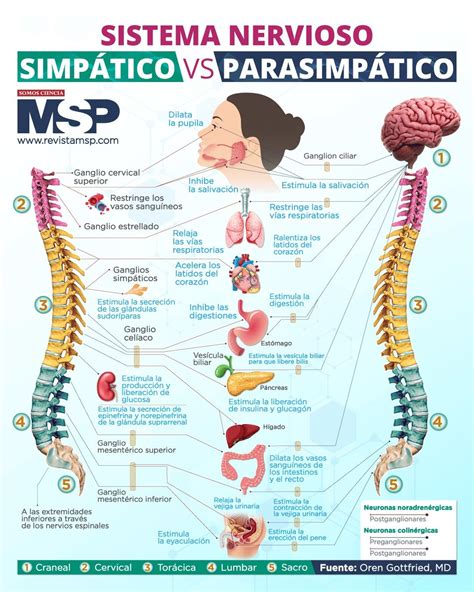
Actualmente, los subtipos de VH se identifican a menudo mediante un manejo ex juvantibus, donde el fracaso de los tratamientos de primera línea guía la búsqueda de mecanismos o etiologías reales. Se proponen enfoques hipotéticos para diferenciar los distintos patrones de VH, apoyando un enfoque "prisma".
El futuro algoritmo de tratamiento de la VH podría basarse en la identificación de los mecanismos fisiopatológicos subyacentes para adaptar el tratamiento a las características de cada paciente. La mayor parte de la elaboración de perfiles de pacientes con VH podría realizarse mediante un registro exhaustivo de antecedentes médicos y una evaluación clínica.
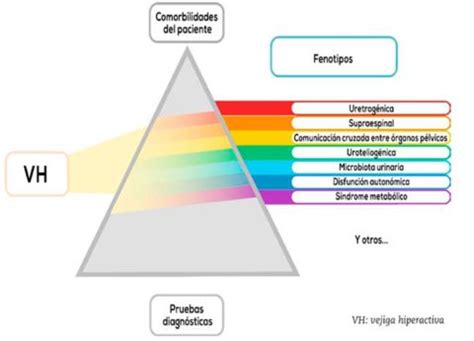
Sistema Nervioso Autónomo: Estructura y Función
El sistema nervioso autónomo (SNA) regula procesos corporales involuntarios, funcionando automáticamente. Se divide en dos ramas principales: el sistema simpático y el sistema parasimpático.
El SNA inerva órganos internos como vasos sanguíneos, estómago, intestino, hígado, riñones, vejiga, pulmones, corazón y glándulas. Después de procesar información interna y externa, el SNA responde estimulando (simpático) o inhibiendo (parasimpático) procesos corporales.
Una vía nerviosa del SNA consta de dos neuronas: una en el tronco encefálico o médula espinal y otra en un ganglio autónomo. Las fibras nerviosas de estos ganglios conectan con los órganos internos. Los ganglios simpáticos se localizan cerca de la médula espinal, mientras que los ganglios parasimpáticos se encuentran cerca o dentro de los órganos.
Funciones del Sistema Nervioso Autónomo
El SNA controla procesos corporales como:
- Presión arterial
- Frecuencia cardíaca y respiratoria
- Temperatura corporal
- Digestión
- Metabolismo
- Balance de agua y electrolitos
- Producción de líquidos corporales
- Micción
- Defecación
- Respuesta sexual
Muchos órganos están controlados predominantemente por uno de los sistemas, aunque a veces ambos sistemas tienen efectos opuestos. Generalmente, el sistema simpático prepara al organismo para situaciones de estrés o emergencia ("lucha o huida"), aumentando la frecuencia cardíaca, dilatando las vías respiratorias, liberando energía almacenada y ralentizando procesos menos importantes como la digestión. El sistema parasimpático, por su parte, se enfoca en la conservación y restauración durante situaciones ordinarias, disminuyendo la frecuencia cardíaca, estimulando el tubo digestivo y restaurando tejidos.
Neurotransmisores del SNA
Los dos mensajeros químicos principales del SNA son la acetilcolina y la norepinefrina. Las fibras nerviosas que secretan acetilcolina se denominan colinérgicas, y las que secretan norepinefrina, adrenérgicas. Generalmente, la acetilcolina tiene efectos parasimpáticos y la norepinefrina, efectos simpáticos, aunque existen excepciones.
Causas de Trastornos del SNA
Los trastornos del SNA pueden ser causados por lesiones en los nervios autónomos o en partes del cerebro que los controlan, o pueden ocurrir sin una causa aparente. Las causas frecuentes incluyen diabetes, trastornos de los nervios periféricos, envejecimiento y enfermedad de Parkinson. Otras causas menos comunes son neuropatías vegetativas, atrofia multisistémica, insuficiencia autónoma pura, trastornos de la médula espinal, trastornos de la transmisión neuromuscular, ciertas infecciones virales (incluyendo COVID-19), lesiones nerviosas y ciertos medicamentos.
Síntomas de Trastornos del SNA
Los síntomas varían según la parte afectada del SNA, pero pueden incluir:
- Mareo o aturdimiento al ponerse de pie (hipotensión ortostática)
- Visión borrosa, presión en la cabeza, palpitaciones, temblores, náuseas, dificultad para respirar
- Pérdida de conciencia
- Disminución o ausencia de sudoración, intolerancia al calor, sequedad ocular y bucal
- Gastroparesia (vaciamiento gástrico lento), con saciedad precoz o vómitos
- Incontinencia urinaria o retención urinaria
- Estreñimiento o incontinencia fecal
- Pupilas que no responden adecuadamente a los cambios de luz
- Disfunción eréctil en varones
SISTEMA NERVIOSO AUTÓNOMO | Qué es, cómo funciona, partes, qué controla y lesiones
Diagnóstico de Trastornos del SNA
El diagnóstico incluye una evaluación médica detallada, pruebas para medir la variación de la presión arterial y la frecuencia cardíaca en diferentes posiciones (incluyendo la prueba de la mesa basculante y la maniobra de Valsalva), examen de las pupilas y pruebas del sudor. También pueden realizarse análisis de sangre y pruebas de imagen para identificar causas subyacentes.
Tratamiento de Trastornos del SNA
El tratamiento se enfoca en abordar la causa subyacente si se identifica, o en aliviar los síntomas. Medidas sencillas como elevar la cabecera de la cama, levantarse lentamente, usar prendas de compresión, aumentar el consumo de sal y agua pueden ayudar. En algunos casos, se emplean medicamentos como fludrocortisona, midodrina o droxidopa para la hipotensión ortostática; oxibutinina, mirabegron, tamsulosina o tolterodina para la incontinencia urinaria; o betanecol para la retención urinaria. Para el estreñimiento, se recomiendan dietas ricas en fibra y laxantes.
Ejercicio Físico y sus Beneficios
El ejercicio físico regular tiene un impacto anatómico y fisiológico significativo en el ser humano. La falta de uso de un órgano tiende a debilitarlo y, con el tiempo, puede llevar a la pérdida de su función. En contraste, el ejercicio fortalece el cuerpo y mejora su funcionamiento.
Beneficios a Nivel Cardiocirculatorio
El ejercicio físico regular mejora la eficiencia del corazón, aumentando la fuerza de contracción y el volumen sanguíneo por latido, lo que resulta en una menor frecuencia cardíaca en reposo. Los vasos sanguíneos periféricos aumentan su calibre, reduciendo la resistencia al flujo sanguíneo y permitiendo que el corazón trabaje a una presión menor. A largo plazo, la presión arterial tiende a disminuir. La capacidad del sistema para transportar oxígeno a los órganos en funcionamiento aumenta, mejorando el rendimiento físico y la tolerancia a la carga laboral y cotidiana.
Adaptaciones Vasculares y Prevención de Enfermedades
Los vasos sanguíneos que irrigan la musculatura esquelética y el corazón experimentan un aumento en número y calibre, lo que ayuda a prevenir o contrarrestar la enfermedad isquémica periférica y miocárdica. El ejercicio programado se considera un factor clave en la prevención de infartos cardíacos, accidentes cerebrovasculares y problemas circulatorios asociados a la enfermedad ateroesclerótica, al ayudar a controlar factores de riesgo como el tabaquismo, la hipertensión, la obesidad y el estrés emocional.
Cambios en la Sangre y el Sistema Respiratorio
El ejercicio regular induce adaptaciones en la sangre, como el aumento de hemoglobina, glóbulos rojos y volumen sanguíneo total, mejorando la capacidad de transporte de oxígeno. Los glóbulos blancos, especialmente los linfocitos, aumentan, reforzando las defensas del organismo. En el sistema respiratorio, la ventilación se vuelve más profunda y lenta, favoreciendo un intercambio gaseoso más efectivo y una mayor incorporación de oxígeno en la sangre. La respiración se vuelve más económica energéticamente.
Adaptaciones Articulares y Musculares
A nivel articular, el ejercicio físico regular mejora la consistencia y distensibilidad de las estructuras periarticulares (tendones, ligamentos, cápsulas articulares), fortaleciéndolas y facilitando una locomoción más efectiva y una mayor resistencia a lesiones. El sistema muscular se ve particularmente beneficiado, con mejoras en la capacitación funcional, el crecimiento estructural y morfológico de las células musculares. El ejercicio es fundamental en la rehabilitación de enfermedades neuromusculares y la recuperación muscular tras inmovilizaciones prolongadas.
Impacto en el Sistema Nervioso
El ejercicio físico mejora la precisión, rapidez y automatización de los movimientos, optimizando la interrelación entre las estructuras del sistema nervioso motor. El sistema nervioso autónomo experimenta un cambio característico con el entrenamiento: el tono simpático se atenúa y el tono parasimpático se acentúa, promoviendo un apaciguamiento de la función de los órganos viscerales. La disminución de los niveles circulantes de adrenalina contribuye a un efecto tranquilizador, siendo el ejercicio una herramienta efectiva para el manejo de la ansiedad.
Las endorfinas liberadas durante el ejercicio actúan como narcóticos fisiológicos, produciendo sensaciones de bienestar, euforia y reduciendo la percepción del dolor. Esto explica el entusiasmo, la tranquilidad y el optimismo que suelen experimentar las personas que se ejercitan regularmente.
Efectos a Nivel Glandular y Metabólico
El ejercicio físico regular influye en las secreciones glandulares, con variaciones en el páncreas que prometen mejoras en la diabetes mellitus, como un aumento de la insulina plasmática y una disminución del glucagón, contribuyendo a reducir los niveles de glucosa circulante. Además, el ejercicio disminuye el colesterol, triglicéridos y lipoproteínas de baja densidad, mientras aumenta la lipoproteína de alta densidad, protegiendo el corazón y las arterias.
Un efecto crónico destacado del ejercicio, especialmente el de resistencia, es la disminución de la grasa corporal, ya que el ejercicio de larga duración quema grandes cantidades de energía, consumiendo calorías almacenadas en forma de grasa y contribuyendo a la pérdida de peso de manera gradual y segura, mientras se capacitan los sistemas orgánicos.
Sistema Nervioso Simpático: Respuesta de Lucha o Huida
El sistema nervioso simpático (SNS), una división del sistema nervioso autónomo, regula involuntariamente acciones como la contracción de músculos lisos y la secreción glandular. Sus efectos son generalmente opuestos a los del sistema parasimpático y están principalmente relacionados con la respuesta de "lucha o huida" ante estímulos externos que amenazan al organismo.
El SNS aumenta la frecuencia y fuerza de los latidos cardíacos, dilata los bronquios, dilata las pupilas, aumenta la presión arterial, dilata los vasos sanguíneos hacia los músculos esqueléticos y estimula la producción de sudor. La estructura del SNS incluye neuronas preganglionares (en encéfalo o médula espinal) y neuronas postganglionares (en ganglios simpáticos).
Acciones del Sistema Nervioso Simpático
- Sistema Cardiovascular: Aumenta la frecuencia y fuerza de las contracciones cardíacas, incrementa la presión arterial al disminuir el calibre de arterias no esenciales para la respuesta de estrés agudo, y dilata las arterias que suministran sangre a los músculos esqueléticos para un mayor trabajo.
- Aparato Digestivo: Disminuye la contracción de los músculos lisos del tubo digestivo, ralentizando la digestión.
- Glándula Suprarrenal: Estimula la producción de adrenalina (epinefrina).
Las terminaciones del SNS liberan noradrenalina y adrenalina, que se unen a receptores específicos (alfa y beta) en los tejidos. Los estímulos emocionales o dolorosos intensos pueden activar el SNS a través del hipotálamo.
Los simpaticomiméticos (ej. adrenalina) estimulan la acción simpática, mientras que los simpaticolíticos la inhiben. La simpatectomía es una intervención quirúrgica para extirpar o destruir ganglios simpáticos con fines terapéuticos.