El cáncer en niños y adolescentes, aunque infrecuente, ha experimentado un aumento gradual en su incidencia general desde 1975. A pesar de esto, se han logrado mejoras notables en la supervivencia, con una disminución de la mortalidad por cáncer infantil superior al 50% entre 1975 y 2020. Sin embargo, el cáncer sigue siendo una causa principal de muerte por enfermedad después de la primera infancia en países como Estados Unidos. Para la leucemia linfoblástica aguda (LLA), una de las formas más comunes, la tasa de supervivencia a 5 años ha aumentado significativamente, superando el 90% en niños menores de 15 años y el 75% en adolescentes.
Los niños y adolescentes sobrevivientes de cáncer requieren un seguimiento minucioso, ya que los efectos secundarios del tratamiento pueden persistir o manifestarse meses o años después. La LLA infantil se origina en los linfoblastos T y B, ubicados en tejidos con células progenitoras hematopoyéticas como la médula ósea y el timo.
Factores de Riesgo y Predisposición Genética en la Leucemia Infantil
La leucemia linfoblástica aguda (LLA) en niños puede estar asociada a diversos factores de riesgo, incluyendo:
- Exposición prenatal a rayos X.
- Exposición posnatal a altas dosis de radiación, como la radioterapia utilizada en el pasado para ciertas afecciones.
- Tratamiento previo con quimioterapia.
- Afecciones genéticas, como el Síndrome de Down.
Leucemia en Niños con Síndrome de Down
En niños con Síndrome de Down, entre el 50% y el 60% de los casos de LLA presentan alteraciones genómicas que afectan al gen CRLF2. Esto generalmente resulta en una sobreexpresión de la proteína CRLF2, que se une al receptor α de la interleucina-7. La fusión P2RY8::CRLF2 es más frecuente en niños con Síndrome de Down y LLA de menor edad, mientras que la fusión IGH::CRLF2 también se observa. Las alteraciones genómicas de CRLF2 son menos comunes (<10%) en niños con LLA-B sin Síndrome de Down y suelen estar relacionadas con el subtipo similar a BCR::ABL1. Estudios retrospectivos han mostrado que la frecuencia de reordenamientos de CRLF2 es significativamente mayor en niños con Síndrome de Down y LLA en comparación con aquellos sin esta condición.
Predisposición Genética Asociada a Síndromes y Alelos Comunes
Existe una mayor predisposición a la LLA asociada a síndromes genéticos, incluso si la leucemia no es la manifestación principal de la afección. Otra categoría de predisposición genética incluye alelos comunes con efectos pequeños identificados mediante estudios de asociación de genoma completo. Estos estudios han revelado varios polimorfismos genéticos de la línea germinal (hereditarios) relacionados con la aparición de LLA infantil. Por ejemplo, los alelos de riesgo de ARID5B se asocian con la formación de LLA-B hiperdiploide. Otros genes con polimorfismos asociados a un mayor riesgo de LLA incluyen GATA3, IKZF1, CDKN2A, CDKN2B, CEBPE, PIP4K2A y TP63.
Factores de Riesgo Genético para LLA-T y LLA-B
Los factores de riesgo genético para la LLA-T se superponen con los de la LLA-B, aunque algunos son específicos. Se ha identificado un alelo de riesgo cerca de USP7 asociado con un mayor riesgo de LLA-T pero no de LLA-B. Este alelo se relaciona con una disminución en la transcripción de USP7, lo que concuerda con hallazgos de variantes somáticas de pérdida de función de USP7 en pacientes con LLA-T. Las variantes germinales y somáticas de USP7 suelen ser mutuamente excluyentes y se observan con mayor frecuencia en pacientes con LLA-T y alteraciones de TAL1. Los factores de riesgo genético que afectan de manera similar la aparición de LLA-B y LLA-T incluyen alteraciones en CDKN2A, CDKN2B y la región 8q24.21 (variantes de la región amplificadora distal cis de MYC).
Predisposición Asociada a Variantes de Alta Penetrancia Poco Frecuentes
Las variantes de la línea germinal que causan cambios patógenos en genes relacionados con la LLA y se observan en familias extensas con LLA familiar (alto tamaño del efecto) constituyen otra categoría de predisposición genética. Muchos de estos genes, como PAX5, ETV6 e IKZF1, desempeñan un papel crucial en el desarrollo de las células B.
- PAX5: En familias con múltiples casos de LLA, se ha identificado una variante patógena de la línea germinal en PAX5 que altera la actividad del gen.
- ETV6: En familias afectadas por trombocitopenia y LLA, se han encontrado múltiples variantes patógenas de la línea germinal en ETV6 que resultan en la pérdida de su función. La secuenciación de ETV6 en muestras de pacientes en remisión ha identificado variantes patógenas relacionadas con LLA en aproximadamente el 1% de los niños evaluados.
- TP53: Las variantes patógenas de la línea germinal en TP53 se asocian con un riesgo elevado de LLA. En un estudio, el 0.7% de los niños con LLA presentaban una variante patógena en TP53, con un riesgo relativo de 5.2 de padecer LLA. La LLA en niños con variantes patógenas de la línea germinal en TP53 se asoció con mayor edad al diagnóstico, hipodiploidía, menor supervivencia específica de la enfermedad (SSC) y supervivencia general, así como un mayor riesgo de segundos cánceres.
- IKZF1: Se han identificado variantes patógenas de la línea germinal en IKZF1 en familias con LLA y en un porcentaje de niños con LLA esporádica. La mayoría de estas variantes afectan negativamente la función del gen.
El Proceso de la Leucemia Linfoblástica Aguda
En la mayoría de los casos, la leucemia linfoblástica aguda (LLA) se desarrolla a través de un proceso de varios pasos que requiere más de una alteración genómica. La alteración genómica inicial puede ocurrir en el útero, y algunos niños que nunca desarrollan LLA nacen con glóbulos sanguíneos poco comunes que presentan una alteración genómica relacionada con la LLA. Los estudios iniciales se centraron en la translocación ETV6::RUNX1, utilizando técnicas como la reacción en cadena de la polimerasa (PCR) para identificar transcritos de ARN que indican la presencia del gen de fusión. La combinación de hallazgos citogenéticos y genómicos, junto con los resultados de la enfermedad residual mínima (ERM), permite definir subgrupos de LLA con tasas de SSC muy altas o muy bajas.
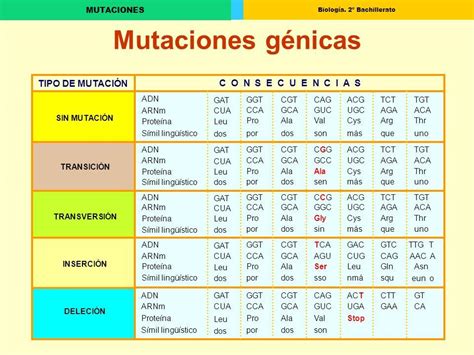
A pesar de los avances en el tratamiento de la LLA infantil, persisten dudas en los ámbitos biológico y terapéutico que deben resolverse para lograr la curación en todos los niños con la menor toxicidad posible. Los ensayos clínicos diseñados para niños y adolescentes con LLA buscan comparar tratamientos estándar con regímenes de investigación para mejorar las tasas de curación o disminuir la toxicidad. Muchos de los avances en la identificación de tratamientos curativos para la LLA infantil y otros cánceres pediátricos han sido el resultado de descubrimientos de investigación y pruebas rigurosas en ensayos clínicos controlados aleatorizados multicéntricos.
Cuidados Paliativos en Leucemia Infantil
Los cuidados paliativos pediátricos se centran en aliviar los síntomas, los efectos secundarios y el estrés en niños y familias que enfrentan una enfermedad grave. Un equipo especialmente capacitado trabaja en conjunto con el equipo médico primario, los pacientes y las familias para planificar la atención. Los cuidados paliativos tempranos son beneficiosos, y se recomienda preguntar al equipo de atención médica sobre estas opciones. El manejo del dolor es una parte fundamental de la atención, y los cuidados paliativos buscan mantener la calidad de vida de los pacientes y sus familias durante una enfermedad grave.
En Chile, el Ministerio de Salud ha desarrollado una red nacional de atención en cuidados paliativos (CP) para niños con cáncer avanzado desde 2003. Este modelo de atención dentro del sistema de salud público ha buscado describir indicadores para la década 2000-2010. Una evaluación retrospectiva de registros clínicos de niños con cáncer avanzado atendidos en CP entre 2003 y 2009 mostró que 484 pacientes y sus familias fueron tratados. La mediana de edad era de 9 años, con predominio de leucemia y tumores del sistema nervioso central (SNC) como diagnósticos más frecuentes. La permanencia promedio en CP fue de 67 días. Se observó una disminución significativa del dolor al momento del fallecimiento (94% con EVA 0-4) y un aumento en el porcentaje de pacientes que fallecen en domicilio, aunque en los últimos años la mitad de los niños fallecen en el hospital.
El Papel de la Atención Primaria en Cuidados Paliativos Pediátricos
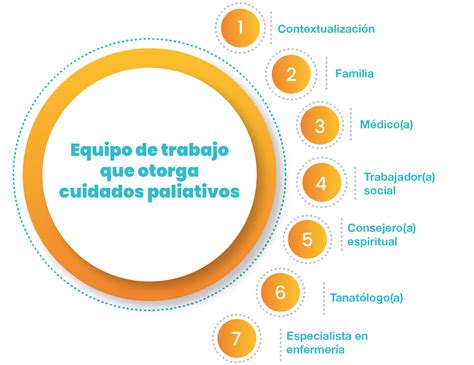
La Atención Primaria (AP) juega un rol crucial como colaborador dentro del equipo multidisciplinario de cuidados paliativos pediátricos. La AP aporta un conocimiento profundo del niño y su familia previo al diagnóstico, durante el seguimiento, y su conocimiento del entorno escolar y social es invaluable. El equipo de CP, compuesto por profesionales como pediatras, enfermeras, químicos-farmacéuticos y psicólogos especializados, trabaja de manera integral, abordando las necesidades físicas, psíquicas, emocionales, sociales y espirituales del niño y su familia.
Comunicación en Cuidados Paliativos Pediátricos
La comunicación efectiva es esencial en los cuidados paliativos pediátricos. Implica un intercambio verbal y no verbal que transmite significado e intencionalidad. Es fundamental adaptar el lenguaje a la edad y estado de ánimo del interlocutor, especialmente cuando se trata de niños. La escucha activa, el respeto por los tiempos del niño y la transmisión de información veraz y comprensible son pilares de una comunicación terapéutica. La coherencia en la información proporcionada por todos los miembros del equipo es vital para evitar confusiones y construir confianza con la familia.
Las habilidades de comunicación con un niño enfermo incluyen:
- Escuchar atentamente y permitir que el niño se exprese.
- No mentir.
- Utilizar términos comprensibles y adaptados.
- Respetar sus creencias y costumbres familiares.
- Hablar con los padres en presencia del niño.
- Evitar frases hechas y vacías.
- Comunicarse con empatía y calidez.
- Responder honestamente a las preguntas del niño, sin ir más allá de lo preguntado.
- Respetar los ritmos y tiempos del niño.
- Reconocer la posibilidad de no tener todas las respuestas.
Proceso de Adaptación a la Enfermedad y la Muerte
La adaptación psicológica a una enfermedad con pronóstico fatal es un proceso complejo que afecta al paciente, su familia y el personal sanitario. La comprensión de la enfermedad y la muerte varía según el desarrollo cognitivo del niño y sus experiencias. Los niños menores de tres años viven la muerte como separación; entre los tres y cinco años, la ven como temporal y reversible; entre los cinco y diez años, toman conciencia de su universalidad e irreversibilidad; y los adolescentes la consideran inevitable e irreversible, aunque con un pensamiento egocéntrico que les impide pensar que pueda ocurrirles a ellos. El afrontamiento de la enfermedad terminal en un niño no puede separarse del proceso familiar, siendo la comunicación del diagnóstico un momento crucial.
El proceso de adaptación suele incluir fases de shock inicial, embotamiento emocional, negación, búsqueda de culpables, rabia, ansiedad, depresión, negociación y, finalmente, aceptación. El tratamiento a menudo conlleva hospitalizaciones, separación de los padres, procedimientos dolorosos y cargas económicas. La fase terminal marca un punto de inflexión, dando inicio al duelo anticipado, con una progresiva despedida y sensación de aislamiento. Los padres en esta etapa necesitan apoyo, cercanía y un espacio para expresar sus temores e inseguridades. El niño, por su parte, requiere seguridad, un ambiente familiar y normalizado, y la libertad de expresar sus sentimientos.
La decisión sobre dónde ocurrirá el fallecimiento del niño (en casa o en el hospital) es importante, siendo el domicilio a menudo preferido, aunque el hospital pueda generar mayor seguridad. La colaboración con los pediatras de Atención Primaria facilita la comunicación y el manejo en el domicilio. La actitud del personal sanitario ante la muerte de un niño también evoluciona, requiriendo autoconocimiento de sus propios sentimientos y actitudes.
Seguimiento y Efectos Tardíos del Tratamiento de Leucemia Infantil
Una vez finalizado el tratamiento para la leucemia infantil, el enfoque principal para muchas familias es la recuperación y el regreso a una vida normal. Los exámenes de seguimiento regulares son cruciales durante varios años después de completar el tratamiento. Estos exámenes generalmente incluyen pruebas físicas, análisis de laboratorio y, en ocasiones, estudios por imágenes. El calendario de seguimiento varía según el tipo de leucemia, el tratamiento recibido y otros factores, siendo más frecuentes al principio y luego espaciándose.
Para los tipos más comunes de leucemia en niños (ALL y AML), la recurrencia de la enfermedad suele ocurrir durante el tratamiento o dentro del primer año posterior a su finalización. Las visitas de seguimiento ofrecen una oportunidad para discutir preguntas y preocupaciones sobre los efectos secundarios del tratamiento, algunos de los cuales pueden ser a largo plazo o manifestarse años después.
Es importante guardar informes médicos importantes del cuidado del niño, ya que pueden ser útiles si hay cambios de médico. Mantener la cobertura de seguro médico también es fundamental. Gracias a los avances médicos, la mayoría de los niños tratados para leucemia viven hasta la edad adulta, pero presentan un riesgo, en cierto grado, de varios efectos tardíos.
Posibles Efectos Tardíos del Tratamiento
- Segundos cánceres: Mayor riesgo de padecer otros tipos de cáncer en el futuro, especialmente tras recibir ciertos medicamentos de quimioterapia como epipodofilotoxinas, agentes alquilantes o antraciclinas.
- Problemas cardíacos y pulmonares: Ciertos medicamentos de quimioterapia o radioterapia en el tórax pueden causar problemas cardíacos o pulmonares a largo plazo. Los riesgos de enfermedad cardíaca y accidente cerebrovascular son mayores en niños tratados para ALL.
- Capacidad de aprendizaje: El tratamiento con radioterapia cerebral o algunos tipos de quimioterapia pueden afectar la capacidad de aprendizaje en algunos niños.
- Crecimiento: Algunos tratamientos pueden afectar el crecimiento, resultando en una estatura adulta ligeramente menor, especialmente después de trasplantes de células madre. El tratamiento con hormona de crecimiento puede ser una opción.
- Fertilidad: El tratamiento del cáncer puede afectar el desarrollo sexual y la capacidad reproductiva futura. Existen opciones para preservar la fertilidad, como la criopreservación de gametos.
El Grupo de Oncología Infantil (Children's Oncology Group o COG) ha desarrollado guías de seguimiento a largo plazo para sobrevivientes de cáncer infantil con el fin de mejorar la atención y el conocimiento sobre los efectos tardíos. Es crucial discutir las posibles complicaciones a largo plazo con los profesionales de la salud y asegurar un plan de seguimiento adecuado.
Problemas Sociales y Emocionales
Los problemas sociales y emocionales pueden surgir durante y después del tratamiento. Algunos niños pueden requerir atención psicológica. La asistencia escolar, siempre que sea posible, es recomendada, y los amigos pueden ser una fuente importante de apoyo. Los programas de reincorporación escolar pueden ser útiles para educar a compañeros y maestros sobre el diagnóstico y tratamiento del cáncer. Los padres y otros miembros de la familia también pueden experimentar dificultades económicas, logísticas y emocionales.
Una vez finalizado el tratamiento, es normal experimentar ansiedad u otras reacciones emocionales. Sin embargo, la preocupación excesiva, la depresión o la molestia pueden afectar negativamente el desarrollo de una persona joven, impactando sus relaciones, desempeño escolar y laboral. Para muchos sobrevivientes, la experiencia del cáncer puede, con el tiempo, ser positiva, permitiendo el desarrollo de valores sólidos.
Programa Cuidados Paliativos Fundación Nuestros Hijos
tags: #metodos #paliativos #leucemia #en #ninos