El mastocitoma es el tumor maligno de piel y tejido subcutáneo más frecuentemente diagnosticado en el perro. Su comportamiento biológico y la supervivencia de los perros pueden ser muy variables, y se han investigado distintos factores para tratar de predecir su agresividad y ofrecer el tratamiento adecuado a cada caso. Actualmente, hay una variedad de pruebas de laboratorio disponibles, aunque no todas tienen el mismo efecto en la predicción del pronóstico.
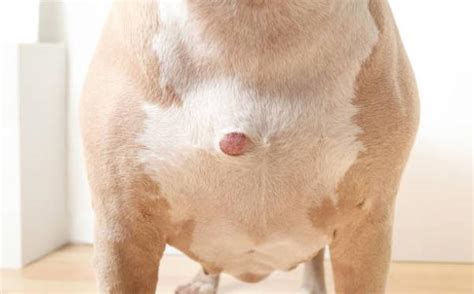
Introducción al Mastocitoma Canino
El mastocitoma canino es un tumor frecuente con un comportamiento clínico y una supervivencia muy variable. Un porcentaje de estos casos se presentan con metástasis a linfonodo regional o a distancia en el momento del diagnóstico. A diferencia de otros tumores, las metástasis a distancia suelen ser en hígado o bazo, y no en pulmones.
Los mastocitos son glóbulos blancos especiales que participan en la respuesta inmunitaria normal. Están presentes en muchos tejidos, pero son especialmente comunes en las zonas de contacto del cuerpo con el exterior, como la piel, las mucosas (tracto respiratorio y digestivo), la conjuntiva y los tejidos nasales. Cuando el cuerpo se expone a diversos efectos nocivos, los mastocitos producen sustancias como la histamina. La histamina desencadena una reacción similar a los síntomas de una alergia, alertando al sistema inmunitario. Lamentablemente, aún se desconocen las causas exactas del mastocitoma canino.
El mastocito es una célula que se origina en la médula ósea, desde donde pasa a la sangre y luego a diferentes tejidos. Los mastocitos tienen un papel importante en la inflamación, en la defensa del organismo y en la cicatrización. Representan un 14-21 % de todos los tumores de piel diagnosticados en perros, según datos del American College of Veterinary Surgeons.
Se presentan habitualmente en pacientes de mediana edad, pero pueden producirse en pacientes de cualquier edad. Algunas de las razas que más se ven afectadas son bóxers, boston terriers, carlinos, cocker spaniels, bull terriers, labrador retrievers, golden retrievers, beagles o schnauzers, entre otras. El mastocitoma canino es una neoplasia cutánea maligna con predisposición genética para ciertas razas como Bóxer, Boston Terrier, Bulldog, Carlino, Labrador, etc. Aparece por igual tanto en perros machos como en hembras y su predisposición aumenta con la edad, aunque también puede darse en animales jóvenes.
La forma de presentación puede asemejarse a cualquier lesión, por este motivo, muchos autores denominan a este proceso neoplásico como “el gran imitador”. En cuanto a su ubicación, la mayor parte de las veces aparece en el tronco, las patas, la cabeza o el cuello. La gran mayoría de los pacientes presentan una sola masa cutánea o subcutánea sin signos externos de enfermedad.
El mastocitoma es el tercer tumor más frecuente en perros y la neoplasia cutánea maligna más prevalente (16-21%) en esta especie. Generalmente los mastocitomas se ven en perros mayores, con una edad media de 8-9 años, pero se han descrito incluso en perros menores de 1 año. Aunque la prevalencia del mastocitoma en el perro es similar en ambos sexos, los machos presentan un 25% más de probabilidad de desarrollar un mastocitoma de alto grado. Las razas, bóxer, golden retriever, bull terrier; bulldog francés, shar-pei y teckel parecen más predispuestas a su padecimiento, mientras lo contrario ocurre en el Yorkshire terrier, pastor alemán, caniche, Chihuahua, y cocker spaniel. Por otra parte, se ha reportado que el riesgo de desarrollar mastocitomas de alto grado es mayor en el shar-pei y en el American Staffordshire terrier y menor en el carlino.
Cualquier masa cutánea o subcutánea que cambie de tamaño debe ser incluida en el diagnóstico diferencial del mastocitoma en perros.
Factores Patológicos y Clasificación
El grado histológico de malignidad ha sido tradicionalmente usado para clasificar los mastocitomas cutáneos. La clasificación de Patnaik de 1984 clasificó los mastocitomas en tres grados:
- Grado I: El 93% de los casos sobrevivieron al menos 4 años.
- Grado II: El 47% de los casos sobrevivieron al menos 4 años.
- Grado III: Solo el 6% de los casos sobrevivieron al menos 4 años.
Esta clasificación predice de forma fiable el pronóstico de la gran mayoría de los mastocitomas de grado I y III, pero no de los de grado II, en los que aproximadamente la mitad tienen un comportamiento biológico agresivo. Además, a la hora de aplicarla se han documentado desacuerdos entre los patólogos.
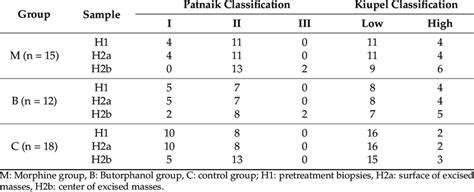
Debido a esta falta de repetibilidad y de capacidad pronóstica para el grado II, un grupo de patólogos propuso una nueva clasificación (Kiupel) donde los mastocitomas son divididos en solo dos grupos: grado bajo o alto. En un estudio, el acuerdo al aplicar la clasificación original de Patnaik fue del 63% para los grados I y II y del 75% para el grado III. Tras evaluar las mismas muestras con la nueva clasificación, el acuerdo entre patólogos fue del 97%. El tiempo libre de enfermedad y la supervivencia fueron significativamente mayores en los de bajo grado (14 meses y 85 meses) que en los de alto grado (8 y 10 meses, respectivamente). Así, la nueva clasificación parece tener menor variabilidad entre patólogos y ofrece buena información pronóstica para ambos grupos.
La combinación de ambas clasificaciones (p. ej., grado II (Patnaik), bajo grado (Kiupel) frente a grado II, alto grado) ayuda a definir mejor el pronóstico de los mastocitomas de grado II. En un estudio, todos los tumores de grado I fueron de grado bajo, y todos los de grado III, de alto grado, por lo que el beneficio en la información pronóstica se observó solamente en los de grado II.
El número total de mitosis en 10 campos de alto aumento (400x) en la zona con mayor actividad mitótica del tumor es una medida indirecta de la proliferación celular. Debe informarse como recuento mitótico y no como índice mitótico. El recuento mitótico tiene la ventaja de que puede realizarse con la tinción rutinaria de hematoxilina-eosina sin ser necesarias técnicas de inmunohistoquímica.
El Ki67 no es un factor necesario para clasificar los mastocitomas como alto o bajo grado. Además, al comparar el recuento mitótico con el índice Ki67, ambos parámetros fueron capaces de identificar los mastocitomas con peor pronóstico de forma independiente de otros factores. Aquellos tumores con recuento mitótico de 6 o más se asociaron con una supervivencia más corta (26% de perros vivos al año del diagnóstico) que los casos con recuento mitótico entre cero y cinco (83% de animales vivos al año). Sin restar importancia a la información que distintos marcadores de proliferación celular puedan ofrecer, es importante tener en cuenta que una información muy similar, en lo que se refiere a su valor pronóstico, puede obtenerse simplemente de un recuento mitótico, sin necesidad de técnicas especiales de tinción.
La proliferación de mastocitos está normalmente regulada por un receptor de la membrana denominado KIT (CD117), presente en los mastocitos y en otras células. Esta proteína KIT está codificada por el protooncogen c-kit. En un estudio, la descripción de una mutación en el gen c-kit ayudó a comprender la causa de algunos de los mastocitomas caninos. Esta mutación provoca una activación continua de las señales de proliferación celular mediante la fosforilación del receptor KIT. La presencia de este receptor puede evidenciarse mediante inmunohistoquímica y se han descrito tres patrones de tinción: localizada en la membrana celular, de forma difusa en el citoplasma y localizada de forma paranuclear, esta última observada en los mastocitomas y las dos primeras en mastocitos normales. Además, se ha observado una relación de estos patrones con el grado histológico del tumor o los índices de proliferación, siendo el patrón citoplasmático o paranuclear más frecuente en tumores más agresivos y el patrón de membrana más común en tumores de bajo grado.
Dado que la activación de KIT es mediante fosforilación de la proteína, se ha investigado si la fosforilación puede usarse como factor pronóstico del comportamiento del tumor o si guarda relación con la presencia de mutación en c-kit. En un estudio, se observó que aunque la presencia de proteína fosforilada (pKIT) se asoció con un peor pronóstico, ésta se identificó tanto en tumores con la mutación como sin ella, por lo que no puede usarse para predecir la presencia de mutación. Además, la existencia de pKIT estaba fuertemente relacionada con otros factores pronósticos como el recuento mitótico o el grado histológico.
Diferentes estudios han evaluado los márgenes quirúrgicos necesarios para una escisión completa del tumor y la relación de estos márgenes con el riesgo de recurrencia local, evidenciando que el riesgo de recurrencia es mayor en tumores de alto grado (incluso con márgenes limpios) que en los de bajo grado. Como ocurre con otros factores descritos, no puede usarse como único parámetro, ya que no todos los tumores extirpados de forma incompleta recurren. La información sobre los márgenes ha de incluirse en el informe de patología siguiendo las recomendaciones publicadas. La descripción tiene que ser detallada e incluir la distancia (mm) entre las células tumorales y el borde quirúrgico, evitando términos ambiguos como estrecho o cercano.
Factores Clínicos y Evaluación
La raza y la edad parecen ser factores importantes en el comportamiento biológico de los mastocitomas, ya que hay razas que se asocian con tumores de alto grado y otras con lesiones de bajo grado. La extensión de la enfermedad en el momento del diagnóstico (estadio clínico) es importante también para el pronóstico. El riesgo de metástasis a linfonodo y a distancia (hígado y bazo) en el momento del diagnóstico es del 30% y el 7%, respectivamente, aunque en algunas localizaciones como el morro, hasta el 58% de los casos tienen metástasis en linfonodo en el momento del diagnóstico. Este riesgo de metástasis depende del grado histológico, siendo del 6%, el 16% y el 50% para los grados I, II y III, respectivamente, y si se usa la clasificación de 2011, del 15% y el 30% para los grados bajo y alto.
Es muy poco frecuente que se observen metástasis a distancia sin que haya metástasis en linfonodos. Es necesaria la citología de hígado y bazo para detectar la presencia de metástasis, ya que la sensibilidad de la ecografía es muy baja. Cambios ecográficos pueden ser debidos a patologías no relacionadas con el mastocitoma y órganos ecográficamente normales pueden presentar metástasis.
El primer paso en la evaluación clínica de una masa con sospecha de mastocitoma es el examen citológico de una muestra obtenida por aspirado con aguja fina. Este examen permite un diagnóstico relativamente preciso en los mastocitomas de bajo grado, por lo que, si el tumor es susceptible de eliminación quirúrgica con márgenes amplios y no hay indicadores pronósticos negativos, la evaluación adicional prequirúrgica puede completarse simplemente con una analítica general y citología del ganglio linfático regional. En caso de indicadores pronósticos negativos, además de esto se indicaría ecografía abdominal y considerar citología hepática y esplénica. La radiología de tórax no es necesaria salvo enfermedad concomitante o para evaluar una posible linfadenopatía esternal. El examen de médula ósea solo se recomienda en pacientes con alteraciones hematológicas que lo sugieran, enfermedad progresiva o recaídas.
Características clínicas: Aproximadamente, el 86-89% de los pacientes se presentan con una masa solitaria principalmente en tronco, región perianal, miembros, cabeza o cuello; mientras que el 11-14% de los casos son de presentación múltiple. Es más probable que masas de crecimiento rápido, mal delimitadas, ulceradas o con lesiones satélites se correspondan con tumores de alto grado. Al mismo tiempo, los tumores de más de 3 centímetros de diámetro, ulcerados o que cursen con signos de enfermedad sistémica tienen mayor probabilidad de metástasis. Se ha propuesto que los que afectan al hocico (especialmente), unión mucocutánea de los labios, región subungueal, perineo, vulva y escroto presentan un comportamiento agresivo. Otros autores opinan que los tumores que afectan al escroto y al plano nasal presentan una mayor probabilidad de ser de alto grado y de metástasis tempranas.
Aproximadamente el 50% de los casos se presentan con signos clínicos relacionados con degranulación de los mastocitos, como la aparición de eritema, edema o pápulas tras la palpación de la zona. Con menor frecuencia pueden presentarse cuadros de hipotensión y colapso circulatorio. Igualmente pueden estar presentes signos digestivos relacionados con presencia de úlceras gástricas/duodenales. Se ha descrito también la presencia de hipereosinofilia como un síndrome paraneoplásico asociado a la liberación de factores quimiotácticos de eosinófilos.
Diagnóstico y Evaluación
Existen principalmente dos métodos para diagnosticar un mastocitoma:
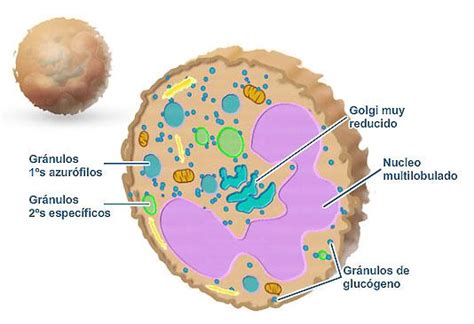
- Citología: mediante una punción o punción-aspiración con aguja fina se toman varias células que permiten diferenciar el mastocitoma debido a la presencia de sus característicos gránulos de sustancias. Es un procedimiento poco doloroso y bien tolerado por el animal ya que es poco invasivo.
- Biopsia: también se puede llegar al diagnóstico mediante la toma de una muestra bajo anestesia general. Resulta necesario realizarla cuando el resultado de la citología no es concluyente o bien para comprobar si los bordes del tumor reseccionado quirúrgicamente están limpios de células tumorales.
El diagnóstico del mastocitoma suele comenzar con la identificación de una masa cutánea o subcutánea en el perro. La confirmación se realiza mediante citología de aspiración con aguja fina (FNA), donde se observan los característicos mastocitos con granulación citoplasmática. Además, es fundamental realizar estudios de imagen, como ecografía y radiografías, para evaluar la presencia de metástasis en órganos como el bazo, el hígado y los ganglios linfáticos.
Aunque el grado histológico representa el factor pronóstico más confiable en el mastocitoma canino, no es capaz de predecir el comportamiento del 100% de los tumores. Por ello, se han investigado distintos marcadores pronósticos (nº de mitosis, índice de proliferación Ki-67, AgNOR, proteína 7 de mantenimiento de microcromosomas, patrón de tinción de la proteína KIT, expresión de c-KIT o el hecho de que el tumor sea solitario o múltiple), si bien ninguno es 100% confiable.
Por otra parte, y desde un punto de vista clínico los mastocitomas pueden clasificarse según los criterios de la OMS (estadios 0 a IV).
Tratamiento del Mastocitoma
Uno de los objetivos principales de la oncología veterinaria es hallar el protocolo de tratamiento más adecuado, ya que puede llegar a ser complicado sobre todo en mastocitomas poco diferenciados.
Tratamiento Quirúrgico
La recomendación generalizada cuando se detecta un mastocitoma canino es la extracción quirúrgica, incluyendo 3 cm tanto alrededor de la masa como en profundidad de la lesión. En general, la cirugía es el tratamiento de elección cuando existen masas solitarias bien delimitadas. Si se sospecha de metástasis, la cirugía deberá incluir la exéresis del ganglio regional afectado. Aunque bien es verdad que la recidiva del tumor es frecuente, y para ello la cirugía debe ser lo suficientemente agresiva para reducir esta reaparición del tumor localmente.
En caso de obtener unos márgenes no libres de tumor, se debe reintervenir la zona para prevenir la aparición descontrolada. En caso contrario de obtener unos bordes limpios con la cirugía, se podría hablar de curación del tumor, pero incluso en estas ocasiones se ha detectado un 30% de recidivas locales.
Siempre y cuando la condición clínica del animal y la localización del tumor lo permitan, la escisión quirúrgica con obtención de márgenes adecuados (2-3 cm lateral y un plano de tejido en profundidad), se considera el tratamiento de elección en el mastocitoma canino. En mastocitomas en estadio II, la extirpación quirúrgica del nódulo linfático regional reduce el riesgo de recaída y la mortalidad, por lo que se ha recomendado la realización de una linfadenectomía durante la cirugía.
Es frecuente que un perro presente múltiples mastocitomas simultáneos y deben considerarse de forma individual en cuanto a su clasificación y comportamiento, salvo que tengamos evidencias de metástasis.
Tratamiento Quimioterápico
Los objetivos del tratamiento quimioterápico son eliminar posibles restos de mastocitoma tras la cirugía si no se dispone de radioterapia o no se puede volver a operar al paciente, mejorar el pronóstico postquirúrgico y controlar las metástasis o la enfermedad sistémica.
Existen múltiples protocolos de quimioterapia con diferentes medicamentos: antiinflamatorios esteroides, inhibidores de ciertas enzimas y combinaciones entre ellos, cuya efectividad será variable en función del tipo de mastocitoma al que nos enfrentemos, la extensión del mismo así como los marcadores que exprese y que los tratamientos pueden inhibir para limitar su crecimiento. Algunos de ellos son prednisona, vinblastina, masitinib, toceranib, lomustina y clorambucilo.
Dado que el comportamiento del mastocitoma es impredecible, es necesario analizar cada caso en particular a la hora de planificar el tratamiento, sabiendo que en muchas ocasiones ningún tratamiento consigue erradicar la enfermedad durante un tiempo prolongado. Y es por ello que el mastocitoma canino sigue siendo un reto para el clínico.
Los corticosteroides son los fármacos que han demostrado una mayor eficacia en el tratamiento del mastocitoma. Son de fácil administración al ser orales, su coste es bajo y los efectos secundarios son notables, siendo lo más destacado la poliuria y la polidipsia. Sin embargo, aunque la mayor parte de los animales manifiestan una respuesta positiva inicial, el tiempo que dura este control del tumor es muy corto. Por ello, sí que puede ser una buena alternativa para la reducción tumoral, previo a un abordaje quirúrgico más seguro.
El masitinib inhibe de forma potente y selectiva la forma mutada del receptor celular c-kit. Aunque es importante saber que no todos los mastocitomas expresan este receptor, es una buena opción de tratamiento, ya sea solo o en combinación con prednisona, puesto que la tasa de respuesta completa es del 65% de los animales tratados y la tasa de supervivencia es del 92% a 24 meses. Durante el tratamiento también hay que controlar posibles trastornos gastrointestinales, la función renal o hepática, aparición de neutropenia, anemia, hipoproteinemias, etc. mediante controles analíticos periódicos. La administración de ambos es oral cada 24-48 h según protocolo utilizado.
Otros quimioterápicos indicados para el mastocitoma canino ofrecen supervivencias similares pero son de administración intravenosa y requieren mayores controles, pudiendo producir más efectos secundarios. El toceranib inhibe la activación del kit tanto natural como mutado, si bien es más efectivo en estos últimos. Los efectos secundarios incluyen también problemas digestivos, neutropenia/trombocitopenia y alopecia.
Otras Terapias
Electroquimioterapia: Es un nuevo tratamiento anticanceroso que combina impulsos eléctricos con fármacos. La tasa de respuesta está en torno al 85% y el tiempo que transcurre hasta que reaparece el tumor está estimado entre 40 y 65 meses.
Radioterapia: Se recomienda en aquellos casos en los que la cirugía no es posible o para tratar los márgenes quirúrgicos “no limpios”. Actualmente solo hay dos centros que trabajen con radioterapia en España (Lugo y Córdoba) y el coste muchas veces puede llegar a ser elevado.
Tratamientos complementarios: Debido a las altas concentraciones de histamina de este tipo de tumores, se recomienda el uso de antihistamínicos H1 (difenhidramina, ciproheptadina, etc.) y H2 (famotidina, ranitidina, cimetidina, etc.) e inhibidores de la bomba de protones (omeprazol, etc.).
En la actualidad, como alternativa al tratamiento quirúrgico, gracias a la colaboración de la empresa de salud animal Virbac con QBiotics, llega al mercado Stelfonta®, especialmente adecuado para casos en que la cirugía es complicada y arriesgada para el animal, ofreciendo al veterinario nuevas opciones de tratamiento. El producto se administra en forma de inyección intratumoral, y está indicado para la eliminación de mastocitomas cutáneos irresecables y no metastásicos en cualquier localización, y subcutáneos no resecables y no metastásicos en el codo o en el corvejón o distales a ellos.
Además de las intervenciones quirúrgicas y oncológicas, la terapia inmunomoduladora está adquiriendo cada vez mayor importancia. En lugar de destruir directamente las células tumorales, activa y fortalece el sistema inmunitario del perro.
La cirugía y la quimioterapia pueden extirpar la mayor parte de la masa tumoral visible, pero no siempre abordan todos los factores subyacentes que intervienen en el desarrollo del cáncer. Cuando la cirugía y la quimioterapia reducen la carga tumoral principal, pueden aliviar el estrés fisiológico del cuerpo. El apoyo al sistema inmunológico juega un papel importante no solo en los tumores de mastocitos en perros, sino también en otros tipos de cáncer, así como en otras afecciones relacionadas con el sistema inmunitario. Por eso, muchos veterinarios enfatizan que el tratamiento suele centrarse en prolongar la vida y mantener la calidad de vida, especialmente en casos más avanzados.
Pronóstico
El pronóstico depende de muchos factores (grado histológico, raza, localización del tumor), pero el mastocitoma en general es impredecible, pudiendo variar de benigno a extremadamente maligno. Algunos estudios han revelado que los carlinos tienen una predisposición a padecer mastocitomas múltiples en más del 50% de los casos. Los tumores localizados en la mitad posterior del cuerpo suelen tener un comportamiento más agresivo de lo que cabría esperar y tienen un menor tiempo libre de enfermedad y menor supervivencia.
Las masas pequeñas que crecen lentamente y permanecen localizadas durante largos periodos de tiempo, tienen mejor pronóstico que los tumores de crecimiento rápido e infiltrativo. El pronóstico lo determina principalmente el grado del tumor, su difusión a otras partes del cuerpo y la dificultad de extirparlo con un amplio margen. Los casos más agresivos, con una diseminación o metástasis avanzada, conllevan un pronóstico desfavorable.
Si el tumor se limita a la piel, no existen signos de metástasis y se extirpa con márgenes limpios, el pronóstico puede ser bastante positivo. El diagnóstico y el tratamiento tempranos mejoran el pronóstico del mastocitoma, por lo que es importante que examines regularmente a tu mascota en casa. Puedes hacerlo de forma sencilla, observándola mientras la acaricias o examinándola intencionadamente.
Debemos tener presente que algunos perros están predispuestos al desarrollo de mastocitomas, por lo que, tras el tratamiento, es muy recomendable un seguimiento estricto con el veterinario, que permita un diagnóstico precoz de nuevos tumores.
La combinación de ambas clasificaciones (p. ej., grado II (Patnaik), bajo grado (Kiupel) frente a grado II, alto grado) ayuda a definir mejor el pronóstico de los mastocitomas de grado II.
Conclusiones: Nunca se debe ignorar la presencia de una masa cutánea/subcutánea en el perro. Aunque en ocasiones puede no tener relevancia clínica, también es posible que se trate de una neoplasia maligna. Por lo tanto, en esa situación siempre se recomienda realizar un aspirado con aguja fina y posterior examen citológico.
tags: #mastocitoma #de #perros #ancianos