El Síndrome de Guillain-Barré (SGB) es la causa más frecuente de parálisis flácida aguda. Se trata de una polineuropatía inflamatoria aguda, generalmente de progresión rápida pero autolimitada, caracterizada por debilidad muscular e hipoestesia distal leve, y su causa se considera autoinmunitaria.
Aunque la forma clásica del síndrome no ha sufrido modificaciones significativas en su comportamiento clínico, el espectro de sus variantes es extenso. Los avances en biología molecular e inmunología han permitido una mejor caracterización de estas formas, destacando el papel de los anticuerpos anti-gangliósidos, que han reestructurado los criterios diagnósticos al aumentar su sensibilidad y especificidad. Los criterios clásicos son insuficientes para una clasificación adecuada y para discriminar los imitadores del síndrome.
La concepción actual de este grupo de neuropatías autoinmunitarias agudas con secuelas crónicas ha impulsado la revisión de los mecanismos fisiopatogénicos, epidemiológicos, inmunológicos y clínicos. Esto obliga a los médicos a clasificar adecuadamente la enfermedad, lo que puede repercutir a largo plazo en la funcionalidad global del paciente y permite diferenciar el "traslape" con otras causas de neuropatía.
SINDROME DE GUILLAIN BARRÉ: Abordaje diagnostico y terapéutico | ENARM - MIR | Mr Doctor Classes
Historia y Epidemiología del Síndrome de Guillain-Barré
La historia del SGB se remonta a 1848, cuando Robert Graves propuso que la parálisis flácida aguda observada en la "epidemié du Paris" tenía su origen en la lesión de los nervios periféricos, distinguiendo por primera vez una parálisis de origen central. En 1858, Jean Baptiste Octave Landry de Thézillat describió formalmente la "Ascending paralysis", conocida hasta 1876 como la parálisis de Landry. Posteriormente, en 1892, Ostler describió seis tipos de polineuropatía y acuñó el nombre de polineuritis aguda febril, sugiriendo que algunos pacientes de Landry probablemente cursaron con un proceso inflamatorio de la médula espinal.
Los casos descritos por Ostler son similares a lo que ahora se conoce como SGB, con la diferencia de que estos últimos no presentan fiebre de manera estricta. En 1916, Guillain, Barré y Strohl describieron las características de la forma clásica del cuadro. En 1958, Miller-Fisher contribuyó con la descripción de una variante consistente en oftalmoplejía, ataxia y arreflexia.
Según metaanálisis realizados en 2011, la incidencia mundial del SGB se estima en 0.89-1.89 casos por 100,000 habitantes/año, con predominio en el género masculino (1.78:1). El 60% de los casos tuvieron previamente un episodio infeccioso, siendo Campylobacter jejuni un agente notable, con reportes de 0.25-0.65 casos por cada 100,000 habitantes/año atribuidos únicamente a este agente. La infección subclínica por citomegalovirus produce 0.6-2.2 casos por cada 100,000 habitantes/año, una relación conocida desde 1967, con predominio de afección de nervios craneales y pérdida auditiva. Algunas series europeas refieren que el 70% de los casos se clasifica como polineuropatía inflamatoria desmielinizante aguda (PIDA) y el 7% como axonal.
Fisiopatología y Clasificación por Anticuerpos Anti-gangliósidos
La fisiopatología del SGB implica una reacción inmunológica, de origen humoral y celular, contra la vaina de mielina de los nervios periféricos, ocasionando su destrucción. Este mecanismo de mimetismo molecular, donde los antígenos de agentes patógenos se asemejan a los gangliósidos de la mielina, es el más comúnmente propuesto para el desarrollo de la enfermedad autoinmune.
Los gangliósidos son glucoesfingolípidos que, cuando presentan uno o más ácidos siálicos en su fracción de carbohidrato, forman parte de las membranas celulares de las células de sostén (glía) del sistema nervioso central y periférico, formadoras de mielina. Estos son blancos moleculares clásicos de los anticuerpos anti-gangliósidos de superficie, que contribuyen al proceso de inflamación-desmielinización del nervio periférico en el SGB.
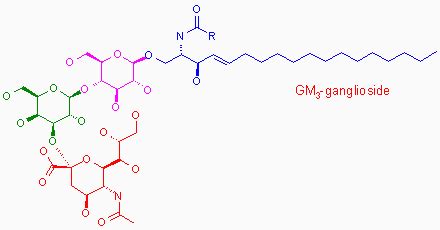
Trabajos de Yuki y colaboradores contribuyeron a caracterizar las variantes del SGB basándose en el antígeno del subtipo gangliósido de mielina contra el que se forma el anticuerpo. Esta clasificación intenta correlacionar el fenómeno autoinmunitario con los hallazgos neurofisiológicos y neuropatológicos descritos. Por ejemplo, en el síndrome de Miller-Fisher y la encefalitis de Bickerstaff, los anticuerpos anti-GQ1b se expresan predominantemente en los nervios abducens, troclear y oculomotor, así como en los husos musculares. El antígeno GT1 se expresa en los nervios glosofaríngeo, vago y en las fibras vagales del nervio accesorio.
El SGB se divide en cinco grandes categorías clínicas: Polineuropatía Desmielinizante Inflamatoria Aguda (AIDP), Polineuropatía Axonal Motora Aguda (AMAN), Polineuropatía Axonal Motora/Sensitiva Aguda (AMSAN), Síndrome de Miller Fisher y la Neuropatía Panautonómica Aguda. También pueden agruparse según sus formas desmielinizantes y axonales.
Criterios Diagnósticos del Síndrome de Guillain-Barré
El diagnóstico del SGB es principalmente clínico. Clásicamente, los criterios diagnósticos del SGB, basados en la cohorte de Asbury y su grupo (1990), incluyen: debilidad progresiva de la musculatura pélvica y braquial, ascendente, con disminución o ausencia de reflejos de estiramiento muscular.
En 2014, el grupo holandés para el estudio del SGB del University Medical Centre Rotterdam emitió los criterios diagnósticos de Brighton del SGB, que reemplazaron a los de Asbury por ser estos últimos poco útiles en la práctica clínica. Los criterios de Brighton ofrecen definiciones de casos explícitas y una clasificación en cuatro niveles de certeza diagnóstica basada en las características del paciente y la información disponible.
Los criterios de Brighton para el diagnóstico de caso confirmado de SGB en adultos con sospecha incluyen: debilidad muscular bilateral y flácida de las extremidades; hiporreflexia o arreflexia en las extremidades con debilidad; patrón de enfermedad monofásica; intervalo de 12 horas a 28 días entre el inicio y la máxima debilidad con meseta clínica posterior; y ausencia de diagnóstico alternativo. Además, se requiere disociación albúmino-citológica en el líquido cefalorraquídeo (nivel de proteínas mayor del normal de laboratorio y <50 células/μl) y hallazgos electrofisiológicos compatibles con SGB.
Estudios Complementarios
- Estudios electrodiagnósticos: Los estudios iniciales de la conducción nerviosa y la electromiografía detectan velocidades lentas de conducción nerviosa y evidencia de desmielinización en dos tercios de los pacientes. Sin embargo, los resultados normales, especialmente en los primeros 5 a 7 días, no excluyen el diagnóstico.
- Análisis del líquido cefalorraquídeo (LCR): Puede detectar disociación albuminocitológica (proteínas aumentadas pero un hemograma normal), aunque puede no aparecer hasta 1 semana y no se observa en el 10% de los pacientes. Se recomienda realizar el estudio del LCR del séptimo al décimo día de evolución.
- Resonancia Magnética (RM): En raras ocasiones, la compresión de la médula cervical puede simular el SGB; en tales casos, debe realizarse una RM.
Escalas de Discapacidad y Pronóstico
Para describir el curso clínico del SGB, se utiliza la escala adaptada de discapacidad de Hughes, la cual es útil para la observación de las fluctuaciones clínicas y durante el tratamiento. Esta escala también se incluye en otras escalas de pronóstico como la Erasmus GBS Respiratory Insufficiency Score (EGRIS) y la Erasmus GBS Outcome Score (EGOS). Estas escalas utilizan el número de días entre el inicio de la debilidad y la admisión hospitalaria, la presencia o ausencia de debilidad facial o bulbar, y la gravedad de la debilidad de las extremidades para predecir la probabilidad de insuficiencia respiratoria y el pronóstico.

Evolución y Complicaciones
En la mayoría de los pacientes, el SGB progresa durante un máximo de una a tres semanas después de la aparición de los síntomas. Dos tercios de los pacientes no pueden caminar de manera independiente al alcanzar la máxima debilidad. La insuficiencia respiratoria ocurre en el 25% de los pacientes, y las principales complicaciones, como neumonía, sepsis, embolia pulmonar y hemorragia gastrointestinal, se manifiestan en el 60% de los pacientes intubados. El 20% de los pacientes gravemente afectados siguen siendo incapaces de caminar seis meses después de la aparición de los síntomas.
Tratamiento del Síndrome de Guillain-Barré
El SGB es una emergencia médica que requiere monitorización constante y soporte de las funciones vitales, generalmente en una unidad de cuidados intensivos. El soporte vital avanzado en la Unidad de Cuidados Intensivos sigue siendo la piedra angular del tratamiento.
Inmunoterapias
Hay dos tipos de inmunoterapia indicadas para el tratamiento del SGB:
- Inmunoglobulina intravenosa (IVIG): Administrada tempranamente, es el tratamiento de elección. Se puede administrar en dosis de 2 g/kg durante 1 a 2 días o 400 mg/kg IV una vez al día durante 5 días consecutivos. La IVIG logra algún beneficio hasta 1 mes después del inicio de la enfermedad.
- Plasmaféresis: Es útil cuando se realiza precozmente y se utiliza cuando la IVIG es ineficaz. Acorta la evolución de la enfermedad, la estadía hospitalaria y reduce el riesgo de mortalidad y la incidencia de parálisis permanente. Sin embargo, puede causar hipotensión y el acceso IV puede ser difícil. La plasmaféresis elimina cualquier IVIG administrada previamente, por lo que no deben combinarse y se recomienda esperar al menos 2 a 3 días después de interrumpir la IVIG.
La combinación de IVIG con esteroides es poco eficaz, e incluso pueden empeorar el pronóstico, por lo que no se recomienda su administración. Un biológico monoclonal humanizado, eculizumab, que previene la activación del complemento, está siendo probado en estudios piloto como el ICA-GBS.
Manejo de Soporte
- Monitoreo respiratorio: La capacidad vital forzada debe medirse con frecuencia. Si es < 15 mL/kg, está indicada la intubación endotraqueal.
- Hidratación y nutrición: Si la ingesta oral es difícil, se administran líquidos IV. Se deben proteger las extremidades de traumatismos y presión.
- Fisioterapia: La terapia con calor ayuda a aliviar el dolor. El movimiento articular pasivo con extensión completa debe iniciarse de inmediato, y los ejercicios activos cuando cedan los síntomas agudos.
- Prevención de trombosis: La heparina de bajo peso molecular (HBPM) subcutánea ayuda a prevenir la trombosis venosa profunda en pacientes encamados.
Pronóstico y Secuelas a Largo Plazo
El SGB es letal en menos del 4% de los casos. La mayoría de los pacientes mejoran considerablemente en un período de meses, pero un número significativo de adultos, y aún más niños, tienen una debilidad residual a los 3 años. Los pacientes con defectos residuales pueden requerir reentrenamiento, dispositivos ortopédicos o cirugía. Después de la mejoría inicial, alrededor del 5% de los pacientes desarrollan una polineuropatía desmielinizante inflamatoria crónica.
Las secuelas comunes incluyen: debilidad muscular persistente, fatiga extrema que puede durar meses o años, dificultades respiratorias en casos graves, problemas de movilidad, problemas sensoriales y dolor crónico (dolor muscular, neuralgia o dolor articular). También pueden presentarse problemas autonómicos, como fluctuaciones en la presión arterial, arritmias cardíacas, estasis gastrointestinal y retención urinaria.
El SGB exige la atención sanitaria de un equipo interdisciplinario, con profesionales capaces de brindar apoyo en los diversos aspectos fisiológicos y mentales alterados, como la nutrición, la respiración y la función corporal.