El retraso mental, también conocido como discapacidad intelectual, es una condición que afecta aproximadamente al 1-3% de la población mundial. En un porcentaje significativo de estos casos, la etiología subyacente permanece desconocida, lo que plantea desafíos importantes en términos de prevención, diagnóstico y manejo. La incertidumbre sobre las causas y la recurrencia del retraso mental tiene profundas repercusiones terapéuticas, sociales y económicas.
La identificación precisa de la causa es fundamental para un diagnóstico certero y la posterior aplicación de pruebas genéticas adecuadas. Con el avance de la tecnología genética y la disponibilidad de nuevas pruebas diagnósticas, la revisión e integración de las guías consensuadas por diversas sociedades científicas (pediátricas, neurológicas y genéticas) se vuelve crucial para abordar el diagnóstico del retraso mental y del retraso del desarrollo.
Definición y Clasificación del Retraso del Desarrollo y Retraso Mental
La expresión retraso del desarrollo se refiere a un déficit de aprendizaje y adaptativo que puede ser significativo y predecir una discapacidad cognitiva o intelectual posterior. Su prevalencia se estima entre el 1 y el 3% de la población.
La clasificación del retraso del desarrollo es clínicamente subjetiva y se reserva habitualmente para niños menores de 5 años, en quienes no es posible realizar una evaluación del cociente intelectual (CI). Los retrasos leves o moderados en estas edades tempranas pueden ser transitorios y no necesariamente predicen un retraso mental futuro, especialmente si afectan a un solo dominio (como el motor o el del lenguaje).
Sin embargo, cuando estos signos se presentan de forma grave o se asocian con otras discapacidades, dismorfias o malformaciones congénitas, se justifica una reevaluación clínica para determinar el abordaje diagnóstico más adecuado. Lamentablemente, debido a la falta de recursos, muchos niños continúan con un diagnóstico de retraso del desarrollo más allá de los 5 años.
El término retraso mental se aplica a niños mayores de 5 años con un CI inferior a 70, confirmado por pruebas estandarizadas. Se caracteriza por una funcionalidad cognitiva significativamente limitada, acompañada de limitaciones adaptativas en al menos dos de las siguientes áreas: habilidades sociales, comunicación, autonomía, salud, trabajo y aprendizaje.
El retraso mental se clasifica generalmente en:
- Leve: CI de 50-70
- Moderado: CI de 35-50
- Grave: CI de 20-35
- Profundo: CI inferior a 20
¿Qué es la discapacidad intelectual?
Etiología Compleja del Retraso Mental y del Desarrollo
La etiología del retraso mental y del retraso del desarrollo es multifactorial, involucrando tanto factores genéticos como ambientales, que pueden actuar de forma aislada o combinada.
Las principales causas identificadas incluyen:
- Anomalías cromosómicas.
- Anomalías del desarrollo del sistema nervioso central (SNC).
- Teratógenos ambientales.
- Retraso mental sociocultural.
- Complicaciones de la prematuridad.
- Enfermedades monogénicas conocidas.
- Causas sindrómicas.
- Enfermedades metabólicas o endocrinas.
Se estima que las causas genéticas podrían estar implicadas en hasta el 50% de los casos de retraso mental o del desarrollo, aunque la confirmación diagnóstica a este nivel sigue siendo un desafío.

Evaluación Clínica y Pruebas Genéticas en el Diagnóstico
Un proceso de evaluación clínica ordenado es fundamental para dirigir de manera eficaz los estudios posteriores en pacientes con retraso mental o del desarrollo. Este protocolo debe incluir una historia clínica detallada, examen físico completo, evaluación neurológica y, en muchos casos, pruebas genéticas.
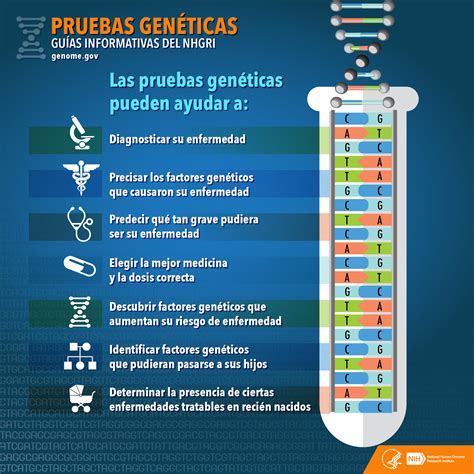
Indicaciones para Pruebas Genéticas
Las pruebas genéticas se indican en las siguientes situaciones:
- Después de haber realizado una exploración básica completa.
- Antecedentes familiares de retraso mental o del desarrollo, abortos o mortinatos sin causa explicada.
- Asociación del retraso del desarrollo o mental con rasgos dismórficos, fenotipo conductual sugestivo, regresión del desarrollo o consanguinidad.
- Descarte de otras causas identificables.
La prescripción de pruebas genéticas debe seguir criterios consensuados para optimizar el esfuerzo diagnóstico y los recursos materiales.
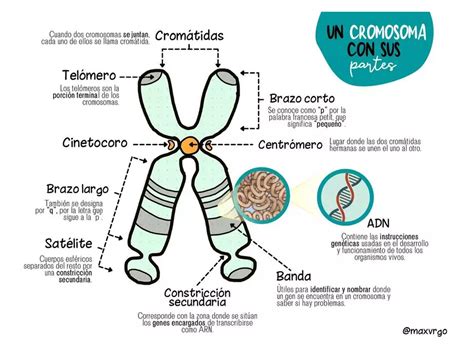
Cariotipo Convencional
El cariotipo convencional ha sido históricamente la herramienta principal para la detección de causas genéticas del retraso mental. Permite un rastreo general del genoma, pero está limitado a la detección de anomalías cromosómicas de gran tamaño (superiores a 5 Mb).
Los estudios cromosómicos son procedimientos sistemáticos importantes en la evaluación, independientemente de la presencia de dismorfias, baja talla o anomalías congénitas. La citogenética sistemática reporta un total de positivos del 3,7%. Estudios de alta resolución (más de 650-850 bandas) no siempre están indicados de forma sistemática, a menos que se investigue una región cromosómica específica o exista una historia familiar de una anomalía sindrómica.
Test para el Síndrome del Cromosoma X Frágil
El estudio molecular de la expansión CGC en el gen FRAXA es una prueba complementaria sistemática debido a su bajo coste y alta prevalencia en pacientes con retraso mental. Según los criterios del American College of Medical Genetics (ACMG), esta prueba resulta positiva en aproximadamente el 2,6% de los casos.
Síndromes de Microdeleción
Las técnicas de hibridación in situ fluorescente (FISH) son particularmente útiles para el diagnóstico de síndromes de microdeleción cuando el paciente presenta características fenotípicas sugestivas. Existen criterios clínicos estandarizados para guiar la prescripción de estudios genéticos dirigidos, como en el caso del síndrome de Angelman o Prader-Willi.
Para el síndrome de Prader-Willi, el análisis FISH es útil para detectar la deleción 15q11-q13 en el 70% de los casos. Si los estudios FISH son normales, se indican estudios de metilación para descartar unidisomía parental o mutaciones en el centro de imprinting.
Dado que un porcentaje significativo de casos de retraso mental o del desarrollo idiopático no presenta un fenotipo característico de síndrome de microdeleción, el abordaje genético mediante FISH con sondas específicas no siempre es posible.
Estudio de las Regiones Subteloméricas
El estudio de las regiones subteloméricas de los cromosomas ha ganado utilidad en el análisis de las causas genéticas del retraso mental o del desarrollo. Se estima que aproximadamente un 5-10% de los casos pueden ser diagnosticados mediante estas técnicas (MLPA subtelomérico o FISH subtelomérico), que ofrecen una resolución mayor que la citogenética convencional.
El grado de retraso del desarrollo o mental, junto con la presencia de dismorfias faciales, anomalías físicas menores, baja talla o microcefalia, son predictores importantes para estos estudios. La presencia de historia familiar positiva o fenotipo peculiar incrementa la probabilidad de detectar anomalías subcromosómicas, que podrían ser responsables del 10% de los casos de retraso mental moderado-grave idiopático.
Se han propuesto criterios de cribado subtelomérico para pacientes con retraso del desarrollo o retraso mental moderado o grave con cariotipo normal, incluyendo historia familiar positiva, pérdidas fetales, historia prenatal de retraso de crecimiento, y características dismórficas.
Microarrays de Hibridación Genómica Comparada (CGH-arrays)
Los microarrays de hibridación genómica comparada (CGH-arrays) son una técnica avanzada para el rastreo de pequeñas pérdidas y ganancias de material genético, permitiendo la identificación de alteraciones inferiores a 1Mb. Estos arrays ofrecen un rastreo de todo el genoma en una sola reacción y podrían diagnosticar un 10% más de casos de retraso mental o del desarrollo que la combinación de estudios citogenéticos convencionales y FISH.
Las recomendaciones actuales del ACMG sugieren limitar el uso de CGH-arrays, en el contexto del retraso mental, a la evaluación de pacientes con anomalías congénitas asociadas, considerando limitaciones de financiación y la posible ambigüedad de los resultados.
Estudios de Genética Molecular
Los estudios de genética molecular permiten dirigir la investigación hacia enfermedades muy específicas. Si bien pruebas como el estudio del síndrome del cromosoma X frágil se utilizan de forma sistemática, la interpretación del tipo de herencia y la clínica del paciente pueden guiar la indicación de tests genéticos para genes específicos implicados en el retraso mental o del desarrollo.
Discapacidad Intelectual: Definición, Etiología y Diagnóstico
La discapacidad intelectual se define por un funcionamiento intelectual significativamente por debajo del promedio (CI < 70-75), combinado con limitaciones en el funcionamiento adaptativo (comunicación, autodirección, aptitudes sociales, etc.). Requiere un soporte variable según la necesidad: intermitente, limitado, amplio o generalizado.
Se considera un trastorno del desarrollo neurológico, apareciendo típicamente en la primera infancia y afectando el desarrollo personal, social, académico y laboral. Las dificultades pueden manifestarse en la atención, memoria, percepción, lenguaje, resolución de problemas o interacción social.
La inteligencia es el resultado de la interacción entre factores genéticos y ambientales. Aunque los niños de padres con discapacidad intelectual tienen un mayor riesgo, la transmisión genética evidente es inusual. La identificación de causas específicas de discapacidad intelectual ha aumentado con tecnologías como el análisis de micromatrices cromosómicas y la secuenciación del exoma.
Factores de Riesgo para la Discapacidad Intelectual
Los factores de riesgo se pueden agrupar en:
- Factores Prenatales: Ocurren durante el desarrollo fetal. El bajo peso al nacer es un factor de riesgo significativo debido a la inmadurez cerebral y orgánica.
- Factores Perinatales: Relacionados con el proceso del parto y el nacimiento. La hipoxia perinatal es una causa frecuente de discapacidad cognitiva, destacando la importancia del tratamiento precoz en recién nacidos prematuros.
- Factores Postnatales: Surgen después del nacimiento. El maltrato infantil (físico y emocional) puede generar retrasos cognitivos. La desnutrición y la privación ambiental en la infancia temprana son causas comunes a nivel mundial.
Las infecciones como encefalitis y meningitis, intoxicaciones (plomo, mercurio) y traumatismos craneoencefálicos graves también pueden provocar discapacidad intelectual.
Signos y Síntomas de la Discapacidad Intelectual
Las manifestaciones primarias incluyen la adquisición lenta de nuevos conocimientos y habilidades, conducta inmadura y limitada capacidad de cuidados personales.
En niños con discapacidad intelectual leve, los síntomas pueden no ser evidentes hasta la edad preescolar. En casos moderados a graves, la detección temprana es más común, especialmente si se asocia con alteraciones físicas o signos de un trastorno subyacente. El retraso del desarrollo suele manifestarse como un retraso en la comunicación. En niños mayores, la combinación de CI bajo y limitaciones en las capacidades de conducta adaptativa es característica.
Los trastornos conductuales son frecuentes y a menudo situacionales, pudiendo ser exacerbados por la falta de entrenamiento en conductas socialmente responsables, límites inconsistentes, deterioro de la comunicación o problemas de salud mental coexistentes.
Trastornos Asociados
Son comunes los trastornos comórbidos, como el trastorno por déficit de atención e hiperactividad (TDAH), trastornos del estado de ánimo, trastornos del espectro autista (TEA), y trastornos de ansiedad. También pueden coexistir deterioro motor o sensitivo (parálisis cerebral, retrasos del lenguaje, hipoacusia), que pueden simular un deterioro cognitivo.
Diagnóstico de la Discapacidad Intelectual
El diagnóstico de la discapacidad intelectual implica una evaluación integral que incluye:
- Pruebas Prenatales: El asesoramiento genético y las pruebas prenatales (amniocentesis, biopsia de vellosidades coriónicas, cribado cuádruple, ecografía) pueden identificar anomalías fetales que predispongan a la discapacidad intelectual.
- Evaluación de la Inteligencia y el Desarrollo: Se utilizan pruebas de inteligencia estandarizadas y pruebas de detección del desarrollo. La evaluación del desarrollo neurológico debe iniciarse ante la sospecha de un retraso.
- Imágenes del Sistema Nervioso Central: La resonancia magnética (RM) craneal puede revelar malformaciones del SNC.
- Estudios Genéticos: El cariotipo estándar, el análisis de micromatrices cromosómicas y los estudios directos de ADN (para el síndrome del X frágil) son herramientas clave. El análisis de micromatrices cromosómicas es la herramienta preferida de investigación.
- Estudios Metabólicos: Manifestaciones clínicas como retraso del crecimiento, letargo, vómitos, convulsiones o rasgos faciales toscos pueden sugerir un trastorno metabólico.
La determinación precisa de la causa es fundamental para el pronóstico, la planificación de programas educativos y de entrenamiento, y el asesoramiento genético familiar.
Factores de Riesgo Específicos y su Asociación con Género
Diversos estudios han investigado la asociación entre factores de riesgo prenatales, perinatales y postnatales y el desarrollo de trastornos del neurodesarrollo, incluyendo el autismo y el retraso mental.
Un estudio realizado en Bogotá (Colombia) analizó 66 historias clínicas de menores diagnosticados con autismo, divididos por género. Se identificaron factores de riesgo significativos asociados al género, como abortos voluntarios, dificultades maternas en embarazos anteriores, intervenciones quirúrgicas durante el embarazo, relaciones parentales conflictivas, actividad física y cognitiva exigentes, consumo de medicamentos, duración del embarazo y peso del neonato. Se observó una mayor cantidad de factores prenatales en varones, mientras que en niñas se registraron más factores perinatales y psicosociales.
La edad materna avanzada ha sido considerada un factor de riesgo para el autismo, aunque los resultados de los estudios son variables. Sin embargo, investigaciones más recientes han asociado significativamente la edad paterna avanzada (mayores de 40 años) con un mayor riesgo de trastornos del espectro autista en sus hijos.
Otros factores de riesgo estudiados incluyen el bajo peso al nacer, el tabaquismo materno recurrente, el tamaño pequeño del feto para la edad gestacional, y calificaciones bajas en el test de Apgar. El parto por cesárea también se ha asociado con diversas condiciones médicas.
El antecedente materno de aborto espontáneo y el sangrado vaginal durante el embarazo han sido reportados como condiciones de alta significatividad. Diversas condiciones obstétricas, como el uso de medicamentos teratógenos, infecciones víricas y la aspiración fetal de meconio, se encuentran estrechamente asociadas a la aparición posterior de autismo y otros TGD.
El estrés materno durante la gestación (tensión y ansiedad marcada) se ha relacionado con una mayor probabilidad de que los hijos experimenten síntomas que puedan desembocar en trastornos neuroconductuales. Sin embargo, la evidencia al respecto aún es objeto de investigación.
Las limitaciones en los estudios de factores perinatales incluyen la delimitación de lo que se considera un factor de riesgo, la variabilidad en los factores analizados y las diferencias metodológicas. El papel del género de los menores afectados frente a la influencia de los factores de riesgo ha sido un elemento de poca discusión, aunque la organización de la información por género puede aportar datos valiosos para la prevención y el tratamiento.
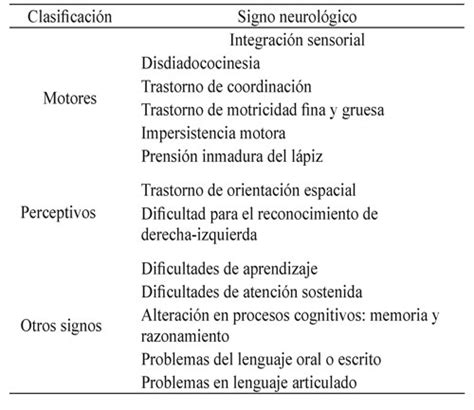
Signos Neurológicos Blandos y Factores de Riesgo
Los signos neurológicos blandos (SNB) se han asociado con dificultades motoras, alteraciones conductuales menores y factores de vulnerabilidad para afecciones como esquizofrenia, TDAH y trastorno disocial. Un estudio descriptivo comparativo investigó la asociación entre factores de riesgo prenatales, perinatales y neonatales y la aparición de SNB en niños de seis a ocho años.
Los resultados indicaron que la presencia de riesgos prenatales, perinatales y neonatales produce alteraciones acumulativas en el desarrollo infantil que pueden asociarse con la aparición de SNB. Signos como la marcha, la agudeza visual y auditiva, y la discriminación izquierda-derecha mostraron diferencias significativas y valores altos en los grupos con riesgo.
En particular, el 90% de los menores con riesgo neonatal presentaron el signo de marcha. La coordinación, el equilibrio y el ritmo son indicadores de la maduración neurológica.
Los menores pertenecientes a estratos socioeconómicos bajos tienen un mayor riesgo de presentar alteraciones en el neurodesarrollo. La edad de la madre en el momento del embarazo, tanto en la adolescencia como después de los 40 años, es un factor de riesgo a considerar.
Los datos obtenidos mediante entrevista semiestructurada y la historia clínica de la Evaluación Neuropsicológica Infantil (ENI-2) revelaron que la mayoría de los participantes fueron producto de la primera o segunda gestación, con una edad media materna de 26,68 años al momento del embarazo. Se observó que un porcentaje significativo de madres tuvieron el embarazo en edades tempranas (16-20 años) o tardías (39-40 años).
Se registraron partos pretérmino y postérmino, así como un nivel educativo predominante entre primaria y bachillerato en la muestra. En cuanto a las condiciones del parto, predominaron los partos naturales, aunque también se reportaron cesáreas. Algunos recién nacidos necesitaron incubadora, oxígeno, y se presentaron casos de sufrimiento fetal o necesidad de uso de fórceps. Las enfermedades neonatales más frecuentes fueron ictericia y cianosis.
La comparación entre grupos mostró que signos como la marcha, la agudeza auditiva y los movimientos de oposición digital se relacionan directamente con el grupo de riesgo al que pertenecen los participantes.